
Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Sindromul Goodpasture: cauze, simptome, diagnostic, tratament
Expert medical al articolului
Ultima examinare: 12.07.2025
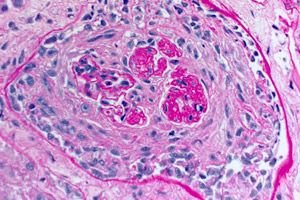
Sindromul Goodpasture este un sindrom autoimun care implică hemoragie pulmonară alveolară și glomerulonefrită cauzată de anticorpi anti-GBM circulanți. Sindromul Goodpasture se dezvoltă cel mai adesea la persoanele cu predispoziție genetică care fumează țigări, dar inhalarea de hidrocarburi și infecțiile virale ale tractului respirator sunt posibili factori suplimentari. Simptomele sindromului Goodpasture includ dispnee, tuse, oboseală, hemoptizie și/sau hematurie. Sindromul Goodpasture este suspectat la pacienții cu hemoptizie sau hematurie și este confirmat prin prezența anticorpilor anti-GBM în sânge. Tratamentul sindromului Goodpasture include schimb plasmatic, glucocorticoizi și imunosupresoare, cum ar fi ciclofosfamida. Prognosticul este bun dacă tratamentul este început înainte de apariția insuficienței respiratorii sau renale.
Sindromul Goodpasture a fost descris pentru prima dată de Goodpasture în 1919. Sindromul Goodpasture este o combinație de glomerulonefrită și hemoragie alveolară în prezența anticorpilor anti-GBM. Sindromul Goodpasture se prezintă cel mai adesea ca o combinație de hemoragie alveolară difuză și glomerulonefrită, dar uneori provoacă glomerulonefrită izolată (10-20%) sau afectare pulmonară (10%). Bărbații sunt afectați mai des decât femeile.
Ce cauzează sindromul Goodpasture?
Cauza bolii nu a fost determinată cu precizie. Se presupune o predispoziție genetică la sindromul Goodpasture, markerul său fiind considerat a fi prezența HLA-DRW2. Există un punct de vedere privind posibilul rol al unei infecții virale anterioare (virusul hepatitei A și alte boli virale), al pericolelor industriale și al medicamentelor (în principal D-penicilamina).
Baza patogenezei sindromului Goodpasture este formarea de autoanticorpi la nivelul membranelor bazale ale capilarelor glomerulare ale rinichilor și alveolelor. Acești anticorpi aparțin clasei IgG, se leagă de anticorpii membranelor bazale în prezența componentei C3 a complementului, cu dezvoltarea ulterioară a inflamației imune a rinichilor și alveolelor pulmonare.
Anticorpii anti-GBM sunt îndreptați împotriva domeniului noncolagenic (NC-1) al lanțului 3 al colagenului de tip IV, care se găsește în cea mai mare concentrație în membranele bazale ale capilarelor renale și pulmonare. Expunerea la factori de mediu - fumatul, infecțiile respiratorii acute virale (ARI) și inhalarea suspensiilor de hidrocarbonat (mai des) - și, mai rar, pneumonia activează prezentarea antigenelor capilare alveolare către anticorpii circulanți la persoanele cu predispoziție ereditară (cel mai adesea acestea sunt purtătoare ale alelelor HLA-DRwl5, -DR4 și -DRB1). Anticorpii anti-GBM circulanți se leagă de membranele bazale, fixează complementul și induc un răspuns inflamator celular, ducând la dezvoltarea glomerulonefritei și/sau a capilaritei pulmonare.
Probabil există o anumită similaritate între autoantigenele membranei bazale a capilarelor glomerulare ale rinichilor și alveolelor. Autoantigenul se formează sub influența efectului dăunător al factorului etiologic. Un factor etiologic necunoscut deteriorează și modifică structura membranelor bazale ale rinichilor și plămânilor. Excreția produșilor de degradare rezultați din membranele bazale glomerulare ale rinichilor încetinește și scade atunci când acestea sunt deteriorate, ceea ce creează în mod natural premisele pentru dezvoltarea leziunilor autoimune la nivelul rinichilor și plămânilor. Încă nu se cunoaște pe deplin care componentă a membranei bazale devine autoantigen. În prezent, se presupune că aceasta este componenta structurală internă a membranei bazale glomerulare a rinichiului, lanțul α3 al colagenului de tip 4.
Complexele imune formate se depun de-a lungul membranelor bazale ale capilarelor glomerulare, ceea ce duce la dezvoltarea unui proces inflamator imun în glomerulul renal (glomerulonefrită) și alveole (alveolită). Principalele celule implicate în dezvoltarea acestei inflamații imune sunt limfocitele T, monocitele, endoteliocitele, leucocitele polimorfonucleare, macrofagele alveolare. Interacțiunea dintre ele este asigurată de mediatori moleculari, citokine (factori de creștere - plachetari, asemănători insulinei, beta-transformanți; interleukina-1, factorul de necroză tumorală etc.). Metaboliții acidului arahidonic, radicalii liberi de oxigen, enzimele proteolitice, moleculele adezive joacă un rol major în dezvoltarea inflamației imune.
Activarea macrofagelor alveolare este de mare importanță în dezvoltarea alveolitei în sindromul Goodpasture. În stare activată, acestea secretă aproximativ 40 de citokine. Citokinele din grupa I (chemotaxine, leucotriene, interleukina-8) sporesc fluxul de leucocite polimorfonucleare în plămâni. Citokinele din grupa II (factori de creștere - trombocite, macrofage) promovează mișcarea fibroblastelor în plămâni. Macrofagele alveolare produc, de asemenea, forme active de oxigen, proteaze, care afectează țesutul pulmonar.
Patomorfologia sindromului Goodpasture
Principalele manifestări patomorfologice ale sindromului Goodpasture sunt:
- afectarea predominantă a patului microcirculator al rinichilor și plămânilor. În plămâni se observă un tablou de venulită, arteriolită, capilarită cu fenomene pronunțate de distrugere și proliferare; afectarea capilarelor se observă în principal în septurile interalveolare, se dezvoltă alveolită cu exudat hemoragic în alveole. Afectarea renală se caracterizează prin dezvoltarea glomerulonefritei proliferative extracapilare cu formarea ulterioară de hialinoză și fibroză, ceea ce duce la dezvoltarea insuficienței renale;
- hemoragii intraalveolare pronunțate;
- dezvoltarea hemosiderozei pulmonare și a pneumosclerozei de diferite grade de severitate, ca urmare a evoluției alveolitei.
Simptomele sindromului Goodpasture
Boala se prezintă cel mai adesea cu manifestări clinice de patologie pulmonară. Hemoptizia este cel mai proeminent simptom; cu toate acestea, hemoptizia poate lipsi în prezența manifestărilor hemoragice, iar pacientul poate prezenta doar modificări infiltrative la radiografia toracică sau un infiltrat și detresă și/sau insuficiență respiratorie. Dispneea (în principal la efort), tusea, starea generală de rău, scăderea capacității de muncă, durerea în piept, febra și pierderea în greutate sunt frecvente. Până la 40% dintre pacienți au macrohematurie, deși hemoragia pulmonară poate preceda manifestările renale cu săptămâni până la ani.
În timpul hemoptiziei, dificultățile de respirație se pot accentua. Slăbiciunea și scăderea capacității de muncă sunt, de asemenea, o preocupare.
Simptomele sindromului Goodpasture variază în timp, de la plămâni limpezi la auscultație până la crepitări și raluri uscate. Unii pacienți prezintă edeme periferice și paloare din cauza anemiei.
În timpul examinării, se observă paloarea pielii, cianoza mucoaselor, pastozitatea sau umflarea pronunțată a feței, scăderea forței musculare și pierderea în greutate. Temperatura corpului este de obicei crescută până la niveluri febrile.
La percuția plămânilor, se poate observa o scurtare a sunetului de percuție în focare extinse de hemoragie pulmonară, dar acest lucru se observă rar; mai des, nu există modificări ale sunetului de percuție.
Un semn auscultator caracteristic al sindromului Goodpasture este respirația șuierătoare uscată și umedă, al cărei număr crește semnificativ în timpul sau după hemoptizie.
La examinarea sistemului cardiovascular, se evidențiază hipertensiune arterială, posibil o creștere a limitei matității cardiace relative spre stânga, sunete cardiace înăbușite, un murmur sistolic ușor și un murmur de fricțiune pericardică, odată cu dezvoltarea insuficienței renale severe. În cazul afectării renale progresive, pe fondul hipertensiunii arteriale semnificative, se poate dezvolta insuficiență ventriculară stângă acută cu imaginea astmului cardiac și a edemului pulmonar. De obicei, această situație se dezvoltă în stadiul terminal al bolii.
De regulă, afectarea renală se manifestă mai târziu, după un anumit timp de la apariția simptomelor pulmonare. Semnele clinice caracteristice ale patologiei renale sunt hematuria (uneori macrohematuria), insuficiența renală cu progresie rapidă, oliguria, hipertensiunea arterială.
În 10-15% din cazuri, sindromul Goodpasture debutează cu semne clinice de patologie renală - apare tabloul clinic al glomerulonefritei (oligurie, edem, hipertensiune arterială, paloare pronunțată), iar apoi se alătură simptome de afectare pulmonară. Mulți pacienți pot prezenta mialgie, artralgie.
Indiferent de variantele de debut, sindromul Goodpasture este în majoritatea cazurilor sever, boala progresează constant, se dezvoltă insuficiență pulmonară și renală severă. Speranța de viață a pacienților de la debutul bolii variază de la câteva luni la 1-3 ani. Cel mai adesea, pacienții decedează din cauza uremiei sau a hemoragiei pulmonare.
Ce te deranjează?
Diagnosticul sindromului Goodpasture
Diagnosticul sindromului Goodpasture necesită detectarea anticorpilor serici anti-GBM prin imunofluorescență indirectă sau, atunci când este disponibil, prin test imunosorbent legat de enzime (ELISA) direct cu NC-1 a3 uman recombinant. Alte teste serologice, cum ar fi testarea anticorpilor antinucleari (ANA), sunt utilizate pentru a detecta LES și titrul antistreptolizinei-O pentru a detecta glomerulonefrita poststreptococică, care poate fi cauza multor cazuri de sindrom pulmonar-renal. ANCA sunt pozitive (în probele periferice) în 25% din cazurile de sindrom Goodpasture. Biopsia renală poate fi indicată dacă este prezentă glomerulonefrita (hematurie, proteinurie, nămol eritrocitar la analiza urinei și/sau insuficiență renală). Glomerulonefrita necrozantă segmentară focală rapid progresivă, cu evoluție progresivă, se găsește la biopsie în sindromul Goodpasture și în toate celelalte cauze ale sindromului pulmonar-renal. Colorația cu imunofluorescență a țesutului renal sau pulmonar relevă în mod clasic depunerea liniară de IgG de-a lungul capilarelor glomerulare sau alveolare. Se observă și în rinichiul diabetic și glomerulonefrita fibrilară, o afecțiune rară care cauzează sindromul pulmonar-renal, dar detectarea anticorpilor GBM în aceste afecțiuni este nespecifică.
Testele funcționale pulmonare și lavajul bronhoalveolar nu sunt diagnostice pentru sindromul Goodpasture, dar pot fi utilizate pentru a confirma prezența hemoragiei alveolare difuze la pacienții cu glomerulonefrită și infiltrate pulmonare, dar fără hemoptizie. Lichidul de lavaj care rămâne hemoragic după spălări multiple poate confirma sindromul hemoragic difuz, în special dacă există o scădere concomitentă a hematocritului.
 [ 3 ]
[ 3 ]
Diagnosticul de laborator al sindromului Goodpasture
- Analiză generală de sânge. Caracteristicile sunt anemia hipocromă feriprivă, hipocromia, anizocitoza, poikilocitoza eritrocitelor. De asemenea, se observă leucocitoză, deplasarea la stânga a formulei leucocitare și o creștere semnificativă a VSH-ului.
- Analiza generală a urinei. În urină se găsesc proteine (gradul de proteinurie poate fi semnificativ), cilindri (granulari, hialini, eritrocitari), eritrocite (poate apărea macrohematurie). Pe măsură ce insuficiența renală cronică progresează, densitatea relativă a urinei scade și se dezvoltă izohipostenurie în testul Zimnitsky.
- Test biochimic de sânge. Niveluri sanguine crescute de uree, creatinină, haptoglobină, seromucoide, a2 și gammaglobuline, conținut scăzut de fier.
- Studii imunologice. Poate fi detectată o scădere a numărului de supresoare de limfocite T, se detectează complexe imune circulante. Anticorpii la membrana bazală a capilarelor glomerulare și alveolare sunt detectați prin imunofluorescență indirectă sau metode radioimunologice.
- Analiza sputei. Sputa conține multe eritrocite, se detectează hemosiderină și siderofage.
Diagnosticul instrumental al sindromului Goodpasture
- Examinarea radiografică a plămânilor. Semnele radiografice caracteristice sunt infiltrate pulmonare în regiunea rădăcinii care se răspândesc în părțile inferioare și mijlocii ale plămânilor, precum și infiltrate progresive, simetrice, bilaterale, asemănătoare norilor.
- Studiul funcției respirației externe. Spirometria relevă un tip restrictiv de insuficiență respiratorie (capacitate vitală scăzută), pe măsură ce boala progresează, se alătură un tip obstructiv de insuficiență respiratorie (scăderea FEV1, indicele Tiffeneau).
- ECG. Se evidențiază semne de distrofie miocardică severă de geneză anemică și hipoxică (reducerea amplitudinii undelor T și a intervalului ST în multe derivații, cel mai adesea în derivațiile toracice stângi). În cazul hipertensiunii arteriale severe, apar semne de hipertrofie miocardică ventriculară stângă.
- Analiza gazelor sanguine relevă hipoxemie arterială.
- Examinarea biopsiilor pulmonare și renale. O biopsie a țesutului pulmonar (biopsie deschisă) și a rinichilor se efectuează pentru verificarea finală a diagnosticului dacă este imposibil să se diagnosticheze cu exactitate boala folosind metode neinvazive. Se efectuează examinarea histologică și imunologică a biopsiilor. Următoarele semne sunt caracteristice sindromului Goodpasture:
- prezența semnelor morfologice de glomerulonefrită (cel mai adesea extracapilară), alveolită hemoragică, hemosideroză și fibroză interstițială;
- detectarea depozitelor liniare de IgG și componentă C3 a complementului pe membranele bazale ale alveolelor pulmonare și glomerulilor renali utilizând metoda imunofluorescenței.
Criterii de diagnostic pentru sindromul Goodpasture
Atunci când se stabilește un diagnostic pentru sindromul Goodpasture, este recomandabil să se utilizeze următoarele criterii.
- O combinație de patologie pulmonară și patologie renală, adică hemoptizie (adesea hemoragie pulmonară), dificultăți de respirație și simptome de glomerulonefrită.
- Evoluție constantă progresivă a bolii, cu dezvoltarea insuficienței respiratorii și renale.
- Dezvoltarea anemiei feriprive.
- Detectarea în timpul examinării radiografice a plămânilor a infiltratelor bilaterale multiple, asemănătoare norilor, pe fondul deformării reticulare a modelului pulmonar.
- Detectarea în sânge a unor titruri ridicate de anticorpi circulanți la nivelul membranei bazale a glomerulilor și alveolelor renale.
- Detectarea depozitelor liniare de IgG și componentă C3 a complementului pe membranele bazale ale capilarelor glomerulare și alveolare.
- Absența altor manifestări sistemice (cu excepția pulmonare și renale).
Diagnosticul diferențial al sindromului Goodpasture
Sindromul Goodpasture trebuie diferențiat de o serie de boli manifestate prin hemoptizie sau hemoragie pulmonară. Este necesar să se excludă afecțiunile oncologice ale bronhiilor și plămânilor, tuberculoza, abcesele pulmonare, bronșiectaziile, bolile cardiace și vasculare (care duc la congestie și hipertensiune arterială în circulația pulmonară), vasculita sistemică, diateza hemoragică.
Programul de screening pentru sindromul Goodpasture
- Analize generale de sânge și urină.
- Analiză biochimică a sângelui: determinarea proteinelor totale și a fracțiilor proteice, creatininei și ureei, transaminazelor, seromucoizilor, haptoglobinei, fibrinei, fierului.
- Analiza sputei: examen citologic, determinarea siderofagelor.
- Studii imunologice: determinarea conținutului de limfocite B și T, subpopulații de limfocite T, imunoglobuline, complexe imune circulante, anticorpi împotriva membranelor bazale ale glomerulilor renali și alveolelor.
- Examinarea cu raze X a plămânilor.
- ECG.
- Spirometrie.
- Examinarea biopsiilor pulmonare și renale.
Ce teste sunt necesare?
Tratamentul sindromului Goodpasture
Tratamentul sindromului Goodpasture include plasmogramă zilnică sau o dată la două zile timp de 2 până la 3 săptămâni (plasmogramă de 4 L) pentru a elimina anticorpii anti-GBM, combinată cu glucocorticoizi intravenoși (de obicei metilprednisolon 1 g timp de cel puțin 20 de minute o dată la două zile de 3 ori cu prednisolon 1 mg/kg greutate corporală zilnic) și ciclofosfamidă (2 mg/kg o dată pe zi) timp de 6 până la 12 luni pentru a preveni formarea de noi anticorpi. Terapia poate fi redusă treptat atunci când funcția pulmonară și renală încetează să se îmbunătățească. Mortalitatea pe termen lung este legată de gradul de insuficiență renală la debutul bolii; pacienții care necesită dializă precoce și cei cu peste 50% nefroni semilunari la biopsie au timpi de supraviețuire mai mici de 2 ani și necesită adesea dializă, cu excepția cazului în care se ia în considerare transplantul renal. Hemoptizia poate fi un semn prognostic bun, deoarece duce la detectarea mai timpurie a bolii; minoritatea pacienților care sunt ANCA-pozitivi răspund mai bine la tratamentul pentru sindromul Goodpasture. Recidiva apare într-un procent mic de cazuri și este asociată cu fumatul continuu și infecțiile tractului respirator. La pacienții cu boală renală în stadiu terminal care au suferit un transplant de rinichi, boala poate recidiva la nivelul grefei.
Care este prognosticul sindromului Goodpasture?
Sindromul Goodpasture este adesea rapid progresiv și poate fi fatal dacă nu este diagnosticat și tratat prompt; prognosticul este bun atunci când tratamentul este început înainte de apariția insuficienței respiratorii sau renale.
Supraviețuirea imediată în momentul hemoragiei pulmonare și al insuficienței respiratorii este asociată cu asigurarea permeabilității căilor respiratorii; intubația endotraheală și ventilația mecanică sunt recomandate pentru pacienții cu niveluri limită ale gazelor sanguine arteriale și insuficiență respiratorie iminentă.

