
Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Schizofrenia
Expert medical al articolului
Ultima examinare: 04.07.2025
Schizofrenia este o tulburare mintală gravă și cronică care afectează gândirea, sentimentele și comportamentul unei persoane. Persoanele cu schizofrenie pot prezenta o varietate de simptome, inclusiv halucinații auditive ( halucinații auditive ), delir (gândire disjunctă sau lipsită de sens), confuzie despre timp și loc și afectare cognitivă. Tulburarea începe de obicei la începutul vieții adulte, adesea în adolescență sau la tinerețe.
Principalele caracteristici ale schizofreniei includ:
- Simptome pozitive: Aceste simptome includ halucinații auditive și vizuale, delir (gânduri și vorbire confuze), idei delirante (convingeri care nu se bazează pe realitate) și tulburări de gândire.
- Simptome negative: Simptomele negative includ apatie, retragere socială, anedonie (incapacitatea de a experimenta plăcere), apraxie (capacitate afectată de a îndeplini sarcinile zilnice) și tulburări de vorbire.
- Dezorganizare: Dezorganizarea implică afectări ale capacității de a menține o secvență logică a gândurilor și o funcție socială și ocupațională normală.
- Simptome cognitive: Acestea sunt tulburări ale funcțiilor cognitive, cum ar fi memoria, atenția și planificarea.
Cauzele schizofreniei nu sunt încă pe deplin înțelese sau cercetate, dar se crede că acestea pot include factori genetici, dezechilibre neurochimice din creier și factori de mediu, cum ar fi stresul, drogurile și expunerea la ele în copilăria timpurie.
Tratamentul schizofreniei implică o combinație de medicație (psihofarmacoterapie) și intervenții psihosociale (psihoterapie, reabilitare și sprijin). Scopul tratamentului este de a reduce simptomele, de a îmbunătăți calitatea vieții și de a gestiona boala. Depistarea și tratamentul precoce pot ajuta la reducerea efectelor schizofreniei și la îmbunătățirea prognosticului.
Epidemiologie
Prevalența globală standardizată în funcție de vârstă a schizofreniei în 2016 a fost estimată la 0,28% (IU 95%: 0,24–0,31), indicând debutul schizofreniei în adolescență și la vârsta adultă tânără, prevalența atingând un vârf în jurul vârstei de 40 de ani și scăzând la grupele de vârstă mai înaintate. Nu s-au observat diferențe de prevalență între sexe.[ 4 ]
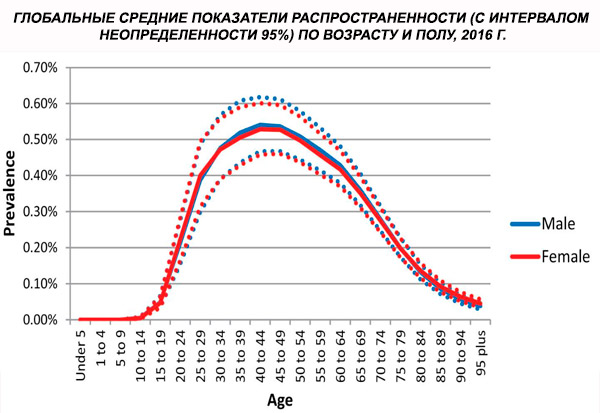
La nivel mondial, prevalența cazurilor a crescut de la 13,1 (IÎ 95%: 11,6–14,8) milioane în 1990 la 20,9 (IÎ 95%: 18,5–23,4) milioane de cazuri în 2016. Grupa de vârstă 25–54 ani.
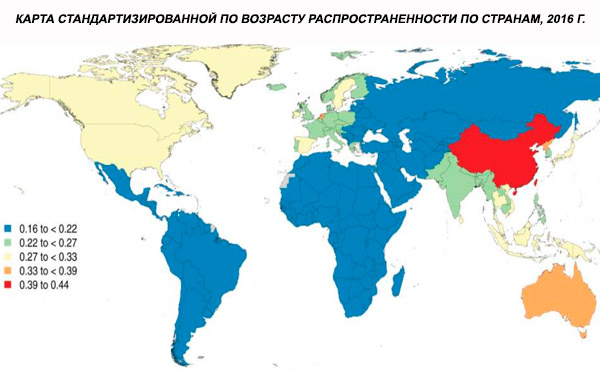
La nivel mondial, prevalența schizofreniei este de aproximativ 1%. Ratele sunt similare în rândul bărbaților și femeilor și sunt relativ constante în diferite culturi. Prevalența este mai mare în rândul claselor socioeconomice inferioare din orașe, posibil din cauza efectelor invalidante ale șomajului și sărăciei. În mod similar, prevalența mai mare în rândul persoanelor singure poate reflecta efectul bolii sau al precursorilor bolii asupra funcționării sociale. Vârsta medie de debut este de aproximativ 18 ani la bărbați și 25 de ani la femei. Schizofrenia începe rareori în copilărie, dar poate apărea la începutul adolescenței și la sfârșitul vieții adulte (uneori numită parafrenie).
 [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
Factori de risc
Apariția medicamentelor psihotrope și a metodelor neurochimice moderne de înaltă sensibilitate a făcut posibilă stabilirea unei legături între funcția sistemului nervos central și tulburările mintale. Cercetările privind mecanismele de acțiune ale medicamentelor psihotrope au permis formularea unui număr de ipoteze cu privire la rolul anumitor neurotransmițători în patogeneza psihozei și schizofreniei. Ipotezele au sugerat implicarea dopaminei, norepinefrinei, serotoninei, acetilcolinei, glutamatului, a mai multor neuromodulatori peptidici și/sau a receptorilor acestora în patogeneza acestor tulburări. Ipoteza dopaminei în schizofrenie a rămas dominantă timp de mai bine de un sfert de secol.
 [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Dopamină
Psihostimulantele, inclusiv cocaina, amfetamina și metilfenidatul, activează sistemul dopaminergic al creierului. Abuzul lor poate provoca psihoză paranoidă, asemănătoare simptomelor pozitive ale schizofreniei. La pacienții cu schizofrenie, psihostimulantele pot provoca o exacerbare a psihozei. În schimb, există dovezi puternice că acțiunea neurolepticelor tipice este asociată cu blocarea receptorilor dopaminergici. În primul rând, majoritatea neurolepticelor tipice pot provoca efecte secundare extrapiramidale, care se pot dezvolta odată cu moartea neuronilor dopaminergici (ca, de exemplu, în boala Parkinson). În al doilea rând, studiile de legare a receptorilor au relevat o relație între eficacitatea clinică a neurolepticelor tipice și afinitatea lor pentru receptorii dopaminergici D2. Mai mult, s-a dovedit că activitatea antipsihotică a neurolepticelor nu depinde de interacțiunea lor cu alți receptori: muscarinici, alfa-adrenergici, histaminici sau serotonini. Toate acestea dau motive să presupunem că simptomele schizofreniei sunt cauzate de stimularea excesivă a receptorilor dopaminergici, probabil în zonele cortico-limbice ale creierului. [ 21 ]
Totuși, punctul slab al ipotezei dopaminei în schizofrenie este că efectul asupra receptorilor dopaminergici afectează în principal simptomele pozitive și are un efect redus asupra simptomelor negative și a tulburărilor cognitive. În plus, nu a fost posibil să se stabilească un defect primar în transmiterea dopaminergică în schizofrenie, deoarece cercetătorii au obținut rezultate diferite atunci când au evaluat funcțional sistemul dopaminergic. Rezultatele determinării nivelului de dopamină și a metaboliților acesteia în sânge, urină și lichidul cefalorahidian au fost neconcludente din cauza volumului mare al acestor medii biologice, ceea ce a nivelat posibilele modificări asociate cu disfuncția limitată a sistemului dopaminergic în schizofrenie.
Creșterea numărului de receptori dopaminergici în nucleul caudat în schizofrenie poate fi considerată, de asemenea, o confirmare a ipotezei dopaminei, însă interpretarea acestor modificări este dificilă și este posibil ca acestea să nu fie atât o cauză, cât o consecință a bolii. [ 22 ] O abordare mai informativă pentru evaluarea stării sistemului dopaminergic se bazează pe utilizarea liganzilor care interacționează selectiv cu receptorii D2 și ne permit să determinăm capacitatea lor de legare. Prin compararea numărului de receptori ocupați înainte și după administrarea medicamentelor, este posibil să se estimeze raportul dintre eliberarea și recaptarea dopaminei. Două studii recente care utilizează tomografia cu emisie de pozitroni (PET), bazate pe această tehnică, au furnizat primele dovezi directe pentru adevărul teoriei hiperdopaminergice a schizofreniei. [ 23 ], [ 24 ]
Măsurarea dopaminei și a metaboliților acesteia în țesutul cerebral la examinarea postmortem poate fi, de asemenea, importantă. Cu toate acestea, deoarece celulele se dezintegrează după moarte, concentrațiile reale de dopamină în țesuturi sunt adesea dificil de determinat. În plus, administrarea de medicamente antipsihotice poate afecta, de asemenea, rezultatele studiilor biochimice postmortem. În ciuda acestor limitări metodologice, studiile postmortem au relevat diferențe neurochimice în creierul pacienților cu schizofrenie și al grupului de control. De exemplu, examinarea postmortem a creierului pacienților cu schizofrenie a relevat concentrații crescute de dopamină în amigdala stângă (parte a sistemului limbic). Această constatare a fost confirmată în mai multe studii și este puțin probabil să fie un artefact (deoarece modificările sunt lateralizate). Creșterea receptorilor postsinaptici de dopamină a fost raportată și în creierul pacienților cu schizofrenie care nu au primit terapie antipsihotică. Aceste date confirmă că numărul crescut de receptori nu este o consecință a terapiei medicamentoase. În plus, există dovezi ale unei creșteri a numărului de receptori D4 de dopamină în anumite zone ale creierului, indiferent dacă pacientul a luat sau nu neuroleptice.
Cu toate acestea, ipoteza dopaminei nu poate explica dezvoltarea manifestărilor abulice și anhedonice ale schizofreniei. După cum am menționat deja, complexul de simptome negative pare a fi relativ independent de simptomele pozitive. Este interesant faptul că agoniștii receptorilor dopaminergici pot influența pozitiv simptomele negative, în timp ce antagoniștii receptorilor promovează dezvoltarea acestora la oameni și le modelează la animalele de laborator. Astfel, deși nivelurile crescute de dopamină în cortexul cingular anterior și în alte structuri limbice pot provoca parțial simptome psihotice pozitive, simptomele negative pot fi o consecință a scăderii activității sistemului dopaminergic în cortexul prefrontal. Poate acesta este motivul pentru care este dificil să se creeze un medicament antipsihotic care să corecteze simultan hiperfuncția dopaminergică în unele zone ale creierului și hipofuncția acestora în altele.
 [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ], [ 31 ]
[ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ], [ 31 ]
Ipoteza glutamatergică a dezvoltării schizofreniei
Glutamatul este principalul neurotransmițător excitator din creier. Interesul privind posibilul său rol în patogeneza schizofreniei a apărut din datele despre complexul receptorilor N-MemuA-D-acuapmame (NMDA), principalul subtip de receptori de glutamat. Studii recente privind interacțiunile dintre sistemele glutamatergic, dopaminergic și GABAergic din creier au arătat că fenciclidina, administrată acut și cronic, este un psihotomimetic care blochează necompetitiv canalul ionic al receptorilor NMDA. Administrarea acută de fenciclidină produce efecte similare cu simptomele pozitive, negative și cognitive ale schizofreniei. În plus, rapoartele privind exacerbarea pe termen lung a psihozei la pacienții cu schizofrenie confirmă proprietățile psihotomimetice ale fenciclidinei. Administrarea pe termen lung a fenciclidinei induce o stare de deficit dopaminergic în cortexul prefrontal, care poate fi responsabilă pentru dezvoltarea simptomelor negative. În plus, atât fenciclidina, cât și analogul său, ketamina, slăbesc transmiterea glutamatergică. Observațiile privind simptomele asemănătoare schizofreniei la consumatorii de fenciclidine sunt confirmate de studii efectuate pe voluntari sănătoși, la care ketamina a indus simptome tranzitorii, ușoare pozitive, negative și cognitive, caracteristice schizofreniei. La fel ca fenciclidina, ketamina a indus distorsiuni ale percepției. Astfel, deficitul de glutamatergică provoacă aceleași simptome ca și în starea hiperdopaminergică, care seamănă cu manifestările schizofreniei. Neuronii glutamatergici sunt capabili să suprime activitatea neuronilor dopaminergici prin intermediul receptorilor NMDA (direct sau prin intermediul neuronilor GABAergici), ceea ce poate explica legătura dintre sistemul glutamatergic și teoria dopaminei în schizofrenie. Aceste date susțin ipoteza care leagă schizofrenia de insuficiența sistemelor glutamatergice. În consecință, compușii care activează complexul receptorilor NMDA pot fi eficienți în schizofrenie. [ 32 ], [ 33 ]
Dificultatea dezvoltării de medicamente care stimulează sistemul glutamatergic constă în faptul că activitatea glutamatergică excesivă are un efect neurotoxic. Cu toate acestea, s-a raportat că activarea complexului receptor NMDA prin intermediul situsului său glicinic de către glicină însăși sau D-cicloserina ameliorează simptomele negative la pacienții cu schizofrenie, ceea ce reprezintă un exemplu excelent de posibilă aplicație practică a ipotezei glutamatergice.
Ipoteza glutamatergică reprezintă o descoperire majoră în studiul tulburărilor biochimice din schizofrenie. Până de curând, studiile neurochimice ale schizofreniei se limitau la studierea mecanismelor de acțiune ale neurolepticelor, care erau dezvoltate empiric. Odată cu creșterea cunoștințelor despre organizarea neuronală a creierului și proprietățile neurotransmițătorilor, a devenit posibilă mai întâi dezvoltarea unei teorii fiziopatologice și apoi crearea de noi medicamente pe baza acesteia. Diversele ipoteze privind originea schizofreniei care există astăzi ne permit să sperăm că, în viitor, dezvoltarea de noi medicamente va continua mai rapid.
Alte ipoteze neurotransmițătoare și neuromodulatoare pentru dezvoltarea schizofreniei
Inervația serotoninergică bogată a cortexului frontal și a sistemului limbic, capacitatea sistemelor serotoninergice ale creierului de a modula activitatea neuronilor dopaminergici și de a participa la reglarea unei game largi de funcții complexe au determinat un număr de cercetători să concluzioneze că serotonina joacă un rol important în patogeneza schizofreniei. De un interes deosebit este ipoteza că excesul de serotonină poate provoca atât simptome pozitive, cât și negative. [ 34 ] Această teorie este în concordanță cu capacitatea clozapinei și a altor neuroleptice de nouă generație care blochează receptorii serotoninei de a suprima simptomele pozitive la pacienții cu boli cronice, rezistenți la neurolepticele tipice. Cu toate acestea, o serie de studii au pus sub semnul întrebării capacitatea antagoniștilor receptorilor serotoninei de a reduce simptomele negative asociate cu psihoza, depresia sau efectele secundare ale farmacoterapiei. Aceste medicamente nu au fost aprobate oficial ca tratament pentru simptomele negative primare care formează defectul subiacent în schizofrenie. Cu toate acestea, ideea că antagoniștii receptorilor serotoninei (în special 5-HT2a) pot fi eficienți a jucat un rol major în dezvoltarea neurolepticelor de nouă generație. Avantajul antagoniștilor combinați ai receptorilor D2/5-HT2 este mai probabil o incidență mai mică a efectelor secundare extrapiramidale decât o activitate antipsihotică mai mare. Cu toate acestea, deoarece acest lucru îmbunătățește complianța (dorința pacienților de a coopera), tratamentul este mai eficient.
Există, de asemenea, ipoteze privind importanța disfuncției sistemelor noradrenergice în schizofrenie. Se presupune că anhedonia este una dintre cele mai caracteristice manifestări ale schizofreniei, care constă în incapacitatea de a primi satisfacție și de a experimenta plăcere, iar alte simptome deficitare pot fi asociate cu disfuncția sistemului de întărire noradrenergică. Cu toate acestea, rezultatele studiilor biochimice și farmacologice care testează această ipoteză s-au dovedit contradictorii. Ca și în cazul ipotezelor dopaminei și serotoninei, se presupune că în schizofrenie poate apărea atât o scădere, cât și o creștere a activității sistemelor noradrenergice.
Ipoteze generale privind dezvoltarea schizofreniei
Cercetările viitoare în domeniul schizofreniei vor fi probabil ghidate de modele complexe bazate pe o sinteză a ipotezelor neuroanatomice și neurochimice. Un exemplu al unei astfel de abordări este o teorie care ia în considerare rolul sistemelor neurotransmițătoare în perturbarea conexiunilor dintre cortex, ganglionii bazali și talamus, care formează circuitele neuronale subcortical-talamocorticale. Cortexul cerebral, prin proiecții glutamatergice către ganglionii bazali, facilitează implementarea unor acțiuni selectate, în timp ce le suprimă pe altele. [ 35 ] Neuronii glutamatergici stimulează neuronii GABAergici și colinergici intercalari, care, la rândul lor, suprimă activitatea neuronilor dopaminergici și a altor neuroni. Studiul mecanismelor neuroanatomice și neurochimice ale circuitelor cortical-subcorticale luate în considerare în acest model a servit ca punct de plecare pentru crearea de noi ipoteze privind patogeneza schizofreniei. Aceste modele facilitează căutarea de ținte neurotransmițătoare pentru medicamente noi și explică, de asemenea, unele dintre caracteristicile acțiunii medicamentelor existente, cum ar fi fenciclidina, în schizofrenie.
Un model neuroanatomic modern a fost propus de Kinan și Lieberman (1996) pentru a explica acțiunea distinctă a antipsihoticelor atipice (cum ar fi clozapina ) în comparație cu agenții convenționali (de exemplu, haloperidolul ). Conform acestui model, acțiunea distinctă a clozapinei se explică prin faptul că are o acțiune foarte specifică asupra sistemului limbic, fără a afecta activitatea neuronilor striatali, în timp ce antipsihoticele tipice au un efect semnificativ asupra funcției striatale. Alte antipsihotice cu proprietăți similare (de exemplu, olanzapina ) pot avea, de asemenea, un avantaj față de agenții convenționali. Antipsihoticele mai noi (de exemplu, risperidona și sertindolul ) nu sunt la fel de limitate la nivelul sistemului limbic ca clozapina, dar se compară favorabil cu antipsihoticele tipice prin faptul că sunt mai puțin susceptibile de a provoca afectări neurologice la doze terapeutice. Cercetările privind validitatea acestei ipoteze și a altora vor continua pe măsură ce devin disponibili noi agenți cu acțiuni farmacologice și clinic similare.
Patogeneza
Pacienților cu schizofrenie li se prescriu anumite grupuri de medicamente, dar alegerea medicamentului este adesea determinată nu atât de diagnostic, cât de simptomele pacientului și de natura combinării lor.
Deși distorsiunea perceptivă și dezorganizarea comportamentală sunt simptome diferite, ele răspund la aceleași medicamente, antagoniștii receptorilor dopaminergici D2. [ 36 ], [ 37 ] Acest lucru justifică luarea în considerare a acestor două complexe de simptome împreună atunci când se discută despre terapia antipsihotică.
Mecanismele de dezvoltare a simptomelor negative în schizofrenie sunt asociate cu scăderea activității sistemului dopaminergic în cortexul prefrontal și nu cu hiperfuncția acestuia în structurile limbice, despre care se presupune că stă la baza psihozei. În acest sens, apar îngrijorări cu privire la faptul că medicamentele care suprimă psihoza pot agrava simptomele negative. [ 38 ], [ 39 ], [ 40 ] În același timp, agoniștii receptorilor dopaminergici pot slăbi simptomele negative, dar pot provoca simptome pozitive. Simptomele negative se numără printre manifestările cheie ale schizofreniei și sunt caracterizate prin tulburări persistente ale sferei emoțional-volitive. Până în prezent, nu există medicamente care să reducă în mod demonstrabil aceste manifestări importante ale bolii. Cu toate acestea, studiile clinice ale antipsihoticelor atipice au arătat că acestea sunt capabile să reducă severitatea simptomelor negative, evaluate folosind scale de evaluare. Scalele SANS, BPRS și PANSS conțin itemi care evaluează activitatea la școală sau la locul de muncă, limitarea contactelor sociale și detașarea emoțională. Aceste simptome pot fi considerate manifestări generale ale bolii, diminuându-se odată cu slăbirea psihozei, dar pot fi asociate și cu efectele secundare ale neurolepticelor (de exemplu, bradikinezie și efect sedativ) sau depresie (de exemplu, anhedonie). Astfel, un pacient cu idei delirante paranoide pronunțate pe fondul terapiei neuroleptice poate deveni mai sociabil și mai puțin precaut, iar reacțiile sale emoționale pot deveni mai vii pe măsură ce simptomele paranoide regresează. Însă toate acestea trebuie considerate ca o slăbire a simptomelor negative secundare și nu ca urmare a unei diminuări a tulburărilor afectiv-volitive primare.
Multe teste neuropsihologice care evaluează atenția și procesarea informațiilor și implică interpretarea neuroanatomică relevă modificări la pacienții cu schizofrenie. Deficiențele cognitive la pacienții cu schizofrenie nu sunt direct legate de principalele simptome ale bolii și, de obicei, rămân stabile chiar și cu o regresie semnificativă a simptomelor psihotice. [ 41 ], [ 42 ] Deficiențele cognitive, împreună cu simptomele negative primare, sunt aparent una dintre cauzele importante ale inadaptării persistente și ale scăderii calității vieții. Lipsa efectului neurolepticelor tipice asupra acestor manifestări centrale ale bolii poate explica un nivel atât de ridicat de dizabilitate la pacienți, în ciuda capacității neurolepticelor de a suprima eficient simptomele psihotice și de a preveni recăderile acestora.
 [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ], [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ]
[ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ], [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ]
Simptome schizofrenii
Conceptul de schizofrenie ca o singură boală a apărut la începutul secolului al XX-lea, când Emil Kraepelin a sugerat că paranoia, hebefrenia și catatonia nu sunt boli separate, ci manifestări ale demenței precoce. De asemenea, el a făcut o distincție clară între această formă de boală mintală și psihoza maniaco-depresivă. Acest lucru a devenit posibil după ce un număr semnificativ de cazuri de boli mintale au fost legate de sifilis, ceea ce a făcut posibilă distingerea lor de restul grupului de pacienți cu tulburări mintale. Descoperirea etiologiei, tratamentului și prevenirii neurosifilisului a fost una dintre principalele victorii ale științei medicale și a dat speranța că vor fi descoperite cauzele principalelor tulburări mintale.
Eugen Bleuler (1950) a propus noul termen „schizofrenie” în locul celui folosit anterior „dementia praecox”, argumentând că fenomenul psihopatologic fundamental caracteristic acestei boli a fost disocierea („scindarea”) - atât „în interiorul” procesului de gândire, cât și între gânduri și emoții. Termenul „schizofrenie” a fost o expresie a acestui concept și, la rândul său, a avut un impact semnificativ asupra dezvoltării sale ulterioare. Formele clasice de schizofrenie (de exemplu, hebefrenică, paranoidă, catatonică, simplă), la care s-au adăugat ulterior schizoafectiva și latentă, sunt încă frecvent diagnosticate în practica clinică în scopuri descriptive, deși recent a existat o tendință de transformare a terminologiei psihiatrice sub influența nomenclaturii oficiale americane DSM-III și DSM-IV. Cu toate acestea, identificarea formelor individuale de schizofrenie s-a dovedit a fi neproductivă în ceea ce privește dezvoltarea unei terapii diferențiate sau studierea etiologiei și patogenezei.
ICD-10 enumeră următoarele simptome ale schizofreniei: idei delirante (bizare, grandioase sau persecutorii), gândire dezordonată (fluxul intermitent sau ilogic al gândurilor sau vorbire incomprehensibilă), tulburări de percepție (halucinații, sentimente de pasivitate, idei de referință), tulburări de dispoziție, tulburări de mișcare (catatonie, agitație, stupoare), declinul personalității și funcționalitate redusă.
Pe parcursul vieții, schizofrenia se dezvoltă la 0,28% (IU 95%: 0,24–0,31). În copilărie, simptomele schizofreniei se manifestă printr-o slăbire a motivației și a reacțiilor emoționale. Ulterior, simțul realității este afectat, iar percepția și gândirea deviază semnificativ de la normele existente într-o anumită cultură, ceea ce se manifestă de obicei prin idei delirante și halucinații auditive. Halucinațiile vizuale și somatice, dezorganizarea gândirii și a comportamentului sunt, de asemenea, frecvente.
Psihoza asociată cu o tulburare a simțului realității se manifestă de obicei la bărbații cu vârsta cuprinsă între 17 și 30 de ani, iar la femei - între 20 și 40 de ani. Evoluția și prognosticul tulburărilor psihotice sunt foarte variabile. La unii pacienți (aproximativ 15-25%), primul episod psihotic se termină cu remisie completă, iar în următorii 5 ani nu există tulburări psihotice (cu toate acestea, în timpul observațiilor ulterioare, proporția acestor pacienți scade). La alți pacienți (aproximativ 5-10%), tulburările psihotice pronunțate persistă fără remisie timp de mulți ani. La majoritatea pacienților, după primul episod psihotic, apare o remisie parțială, iar ulterior se observă periodic exacerbări ale simptomelor psihotice.
În general, în timp ce severitatea tulburărilor psihotice atinge un platou la 5-10 ani de la primul episod, sărăcirea emoțional-volitivă continuă pentru o perioadă mai lungă. [ 53 ] Progresia simptomelor schizofreniei este adesea o consecință a creșterii tulburărilor primare asociate cu schizofrenia. Acestea includ autismul, pierderea capacității de muncă, dificultăți de învățare și stimă de sine scăzută și a celorlalți. Drept urmare, pacienții sunt lăsați singuri, incapabili să găsească un loc de muncă și supuși stresului, ceea ce poate provoca o exacerbare a simptomelor și o creștere a deficienței lor funcționale. În plus, diagnosticul de schizofrenie în sine continuă să genereze o reacție negativă, printre altele, ceea ce limitează și mai mult capacitățile pacientului. Deși odată cu vârsta există o tendință ca simptomele schizofreniei să slăbească și starea funcțională să se îmbunătățească adesea, aceasta nu poate compensa anii de viață pierduți de pacient și oportunitățile ratate.
Relația dintre activitatea criminală și schizofrenie
Wessely și colab., în studiul lor asupra Registrului Camberwell, au căutat să răspundă la întrebarea: „Este schizofrenia asociată cu un risc și o frecvență crescute ale infracțiunilor?” Aceștia au concluzionat că persoanele cu schizofrenie, deși nu sunt în general considerate a prezenta un risc crescut de comportament infracțional, prezintă un risc mai mare decât alte tulburări mintale de condamnare pentru infracțiuni violente. A existat un risc crescut de violență și, prin urmare, de condamnare pentru violență în rândul persoanelor cu psihoză, dar această asociere a fost mai puțin clară în absența consumului excesiv de substanțe comorbide. Într-o analiză a morbidității psihiatrice la deținuți, realizată de Oficiul Național de Statistică, prevalența psihozei funcționale în anul studiat a fost de 7% în rândul bărbaților condamnați, 10% în rândul bărbaților necondamnați în arest preventiv și 14% în rândul deținuților, comparativ cu o cifră comparabilă de 0,4% în populația generală. Rezultatele acestei analize pot necesita o reconsiderare a rezultatelor de mai sus, deoarece este foarte puțin probabil ca diferențele în ratele tulburărilor mintale dintre populațiile penitenciare și cele generale de această dimensiune să poată fi explicate prin părtinirea instanțelor de a condamna persoanele cu boli mintale. Desigur, aceste rezultate nu indică în niciun fel o relație cauzală între criminalitate și psihoză, ci doar o asociere.
Asocierea schizofreniei cu infracțiunile violente a primit, în general, mai multă atenție decât asocierea schizofreniei cu alte infracțiuni. [ 54 ], [ 55 ] Analiza cercetărilor pe această temă realizată de Taylor concluzionează că, la persoanele cu schizofrenie și condamnate pentru infracțiuni violente, actele violente apar în mod covârșitor după debutul bolii. Un studiu asupra schizofreniei cu primul episod arată că, printre pacienții cu primul episod, mai mult de o treime au avut un comportament violent în luna dinaintea internării, inclusiv comportamente care le pot pune viața în pericol și comportamente sexuale bizar. Mulți dintre acești pacienți avuseseră contact cu poliția înainte de prima lor internare, dar puțini au fost acuzați după internare. Taylor a investigat posibilitatea schizofreniei într-un eșantion consecutiv de deținuți aflați în arest preventiv în închisoarea Brixton. Prevalența condamnărilor pentru infracțiuni violente în rândul persoanelor cu schizofrenie a fost de aproximativ 12% până la 13%. Aproximativ 5% până la 8% dintre subiecții de control au fost condamnați pentru infracțiuni violente. Conform unui raport al Anchetei Naționale Confidențiale privind Omuciderile comise de Persoanele cu Boli Mintale, 5% dintre cei condamnați pentru omucidere au prezentat simptome de psihoză. Contrar credințelor populare despre persoanele cu psihoză, victima este cel mai adesea un membru al familiei, mai degrabă decât un străin (o constatare mai generală pentru comportamentul violent într-un eșantion comunitar în studiul Steadman și colab.).
Unele simptome specifice ale schizofreniei sunt asociate cu violența. Astfel, Virkkunen, studiind un grup de pacienți schizofrenici din Finlanda care s-au făcut vinovați de episoade severe de violență și un grup de incendiatori, a constatat că 1/3 dintre aceștia au comis infracțiuni direct ca urmare a halucinațiilor sau a iluziilor; restul de 2/3 au comis infracțiuni din cauza problemelor cauzate de stresul din familie. Simptomele amenințării/pierderii controlului asupra situației sunt direct asociate cu violența. În cazul simptomelor care distrug sentimentul de autonomie personală și capacitatea de a influența situația, pacienții pot considera justificate acțiunile lor de contracarare a amenințărilor legate de ei („raționalitate în cadrul iraționalității”).
Pacienții psihotici deliranți care comit acte violente ca urmare a ideilor lor diferă de pacienții non-violenți prin preocuparea lor cu dovezile care să le susțină ideile, convingerea că astfel de dovezi au fost găsite și modificările afective, în special depresia, furia sau frica, asociate cu preocuparea lor delirantă. În studiile Brixton realizate de Taylor și colab., ideile delirante de pasivitate, ideile delirante religioase și ideile delirante de influență au fost semnificativ mai asociate cu acte violente.
Riscul asociat cu simptomele active ale schizofreniei, inclusiv simptomele de amenințare/pierdere a controlului, este mult crescut de abuzul de substanțe. Rolul acestui din urmă factor este evidențiat de studiul realizat de Steadman și colab.: atunci când acest factor a fost controlat, rata violenței în rândul pacienților psihiatrici recent externați nu a fost mai mare decât rata violenței în populația generală. Halucinațiile ca parte a bolii sunt cel mai adesea asociate cu violența dacă sunt halucinații de comandă sau dacă gusturile și mirosurile percepute în mod fals sunt interpretate ca „dovezi” pentru idei delirante de control. Mai puțin bine înțeles este rolul dezvoltării anormale a personalității în comiterea infracțiunilor de către persoanele cu schizofrenie (fie că este o afecțiune comorbidă, fie o consecință a bolii).
 [ 56 ], [ 57 ], [ 58 ], [ 59 ]
[ 56 ], [ 57 ], [ 58 ], [ 59 ]
Teorii ale simptomelor schizofreniei
Conceptul original de schizofrenie ca boală neurodegenerativă cu debut precoce și progresie constantă (dementia praecox) este în prezent respins. Ipotezele moderne consideră schizofrenia ca o boală de neurodezvoltare asociată cu dezvoltarea deficitară a sistemului nervos și care progresează doar în primii ani, dar nu pe tot parcursul vieții, ceea ce este mai consistent cu observațiile clinice. [ 60 ], [ 61 ] Teoria disontogenetică a schizofreniei ne permite să înțelegem rolul factorilor etiologici stabiliți. Factorii de risc pentru schizofrenie, cum ar fi nașterea iarna, antecedentele familiale pozitive, sarcina și nașterea complicate, pot perturba dezvoltarea creierului, formând precoce o predispoziție la boală. Observațiile copiilor cu predispoziție ereditară, de exemplu, cei născuți din mame care suferă de schizofrenie, au relevat o legătură între prezența tulburărilor motorii, cognitive și afective și dezvoltarea ulterioară a psihozei. Există dezbateri cu privire la faptul dacă psihoza este rezultatul progresiei bolii în copilărie și adolescență sau dacă apare atunci când o predispoziție care a apărut în primii ani, dar a rămas stabilă, se manifestă în timpul adolescenței, în condiții de stres psihologic crescut. Aceste teorii nu se exclud reciproc, deoarece ambele sugerează apariția precoce a unor simptome ușoare și dezvoltarea ulterioară a psihozei complete. Trebuie menționat că, după ce boala a atins nivelul psihotic, nici metodele de neuroimagistică, nici cercetările neuropsihologice, nici observația clinică și nici, în final, datele patomorfologice nu indică o progresie ulterioară a bolii.
Majoritatea pacienților cu schizofrenie continuă să prezinte simptome negative pe tot parcursul vieții, iar creșterea inadaptării sociale poate fi o consecință a relației dintre pacient și societate. [ 62 ] Acest lucru poate fi explicat la un nivel foarte elementar, de exemplu, luând în considerare problema ocupării forței de muncă. După un episod psihotic, pacientului îi este dificil să se întoarcă la viața și ocupația anterioară. Chiar și în absența oricăror simptome, angajatorii, colegii, prietenii și rudele nu îl consideră o persoană capabilă. Rata șomajului în rândul pacienților cu schizofrenie ajunge la 80%, deși o proporție semnificativă dintre aceștia își păstrează capacitatea de muncă. Semnificația acestui factor este bine demonstrată în studiile asupra culturilor sociocentrice din țările în curs de dezvoltare, unde pacienții cu schizofrenie își pot menține statutul social și profesional într-un mediu semnificativ mai puțin stresant. În aceste țări, boala are o evoluție mai benignă. O discuție detaliată despre etiologia și fundamentele neurobiologice ale schizofreniei este oferită de Carpenter și Вuchanan, Waddington.
De mult timp s-a observat că pacienții cu schizofrenie sunt foarte eterogeni în ceea ce privește natura debutului bolii, simptomele principale, evoluția, eficacitatea tratamentului și rezultatul. În 1974, a fost propusă o ipoteză alternativă (Strauss și colab., 1974), bazată pe date din observații clinice transversale și prelungite, care indică o independență relativă între simptomele psihotice pozitive, simptomele negative și o încălcare a relațiilor interpersonale. Esența ipotezei este că aceste grupuri de simptome au o bază psihopatologică independentă și nu reprezintă manifestări ale unui singur proces fiziopatologic. [ 63 ] În perioada de observație, s-a observat o corelație ridicată între severitatea simptomelor psihopatologice legate de un grup și, dimpotrivă, nu s-a observat nicio corelație între severitatea simptomelor legate de diferite grupuri. Aceste date au fost confirmate în numeroase studii, dar cu o singură adăugare. S-a dovedit că halucinațiile și ideile delirante sunt strâns legate între ele, dar nu se corelează cu alte simptome pozitive (de exemplu, dezorganizarea gândirii și a comportamentului). În prezent, este în general acceptat faptul că manifestările cheie ale schizofreniei includ o distorsiune a simțului realității, dezorganizarea gândirii și a comportamentului, simptome negative și afectarea cognitivă. Simptomele negative ale schizofreniei includ slăbirea reacțiilor emoționale și a manifestărilor lor externe, sărăcia vorbirii și scăderea motivației sociale. Anterior, Kraepelin a descris aceste manifestări ca fiind „secarea sursei voinței”. Diferențele dintre grupurile de simptome sunt extrem de importante atunci când se prescrie farmacoterapia. Alte manifestări clinice importante din punct de vedere terapeutic includ depresia, anxietatea, agresivitatea și ostilitatea, comportamentul suicidar.
Timp de mulți ani, efectul medicamentelor în schizofrenie a fost evaluat în principal prin efectul lor asupra simptomelor psihotice sau a parametrilor înrudiți, cum ar fi durata spitalizării sau a remisiunii. Odată cu recunoașterea independenței relative a diferitelor grupuri de simptome, o evaluare cuprinzătoare a efectului terapiei asupra fiecăruia dintre aceste grupuri a devenit standard. S-a dovedit că terapia antipsihotică standard nu are practic niciun efect asupra deficiențelor cognitive și a simptomelor negative ale schizofreniei. [ 64 ] Între timp, aceste două grupuri de simptome pot avea o influență decisivă asupra severității stării pacientului și a calității vieții acestuia. Conștientizarea limitelor farmacoterapiei tradiționale a devenit un impuls pentru dezvoltarea de noi agenți pentru tratamentul acestor manifestări ale schizofreniei.
Schizofrenia este o boală cronică care poate progresa pe parcursul mai multor exacerbări, deși durata și caracteristicile exacerbărilor pot varia. Pacienții cu schizofrenie tind să dezvolte simptome psihotice cu 12 până la 24 de luni înainte de a solicita tratament. Perioada premorbidă poate include competență socială normală sau afectată, dezorganizare cognitivă ușoară sau distorsiuni perceptive, capacitate scăzută de a experimenta plăcere (anhedonie) și alte dificultăți generalizate de adaptare. Astfel de simptome ale schizofreniei pot fi subtile și recunoscute doar retrospectiv sau pot fi mai proeminente odată cu afectarea funcționării sociale, academice și ocupaționale. Simptomele subclinice pot fi prezente în perioada prodromală, inclusiv retragere sau izolare, iritabilitate, suspiciune, gânduri neobișnuite, distorsiuni perceptive și dezorganizare. Debutul bolii (idei delirante și halucinații) poate fi brusc (în decurs de zile sau săptămâni) sau lent și gradual (în decurs de ani). Evoluția schizofreniei poate fi episodică (cu exacerbări și remisiuni evidente) sau continuă; există o tendință ca deficitul funcțional să se agraveze. În faza avansată a bolii, tiparele bolii pot fi stabile, gradul de dizabilitate se poate stabiliza și chiar scădea.
În general, simptomele schizofreniei ca atare pot fi împărțite în simptome pozitive, negative, cognitive și dezorganizatorii. Simptomele pozitive sunt caracterizate prin excesul sau distorsiunea funcțiilor normale; simptomele negative sunt caracterizate printr-o scădere sau pierdere a funcțiilor normale. Simptomele dezorganizatorii includ tulburări de gândire și comportament inadecvat. Simptomele cognitive sunt tulburări de procesare a informațiilor și dificultăți în rezolvarea problemelor. Tabloul clinic poate include simptome din una sau toate aceste categorii.
Simptomele pozitive ale schizofreniei pot fi împărțite în idei delirante și halucinații, sau tulburări de gândire și comportament inadecvat. Idei delirante sunt credințe false. În ideile delirante de persecuție, pacientul crede că este hărțuit, urmărit sau înșelat. În ideile delirante de referință, pacientul crede că pasaje din cărți, ziare, versuri de cântece sau alte indicii externe sunt relevante pentru el. În ideile delirante de inserare sau retragere a gândurilor, pacientul crede că alte persoane îi pot citi gândurile, că gândurile sale sunt transmise de alții sau că gândurile și impulsurile îi sunt implantate de forțe externe. Halucinațiile pot fi auditive, vizuale, olfactive, gustative sau tactile, dar halucinațiile auditive sunt de departe cele mai frecvente. Pacientul poate auzi voci comentând comportamentul său, vorbind între ele sau făcând remarci critice și insultătoare. Idei delirante și halucinațiile pot fi extrem de stresante pentru pacient. [ 65 ]
Tulburările de gândire includ gândirea dezorganizată cu vorbire incoerentă, fără scop, cu treceri constante de la un subiect la altul. Tulburările de vorbire pot varia de la o ușoară dezorganizare la incoerență și lipsă de sens. Comportamentul inadecvat poate include prostie copilărească, agitație și aspect și maniere inadecvate. Catatonia este o formă extremă de tulburări de comportament care poate include menținerea unei posturi rigide și rezistență persistentă la mișcare sau activitate motorie spontană fără scop.
Manifestările negative (deficitare) ale bolii se exprimă sub formă de afect aplatizat, sărăcie de vorbire, anhedonie și nesociabilitate. În cazul afectului aplatizat, fața pacientului apare hipomimetică, cu contact vizual slab și expresivitate insuficientă. Sărăcia de vorbire se manifestă printr-o scădere a producției de vorbire, răspunsuri monosilabice la întrebări, creând impresia de gol interior. Anhedonia poate reflecta un interes insuficient pentru activitate și o creștere a activității fără scop. Nesociabilitatea se manifestă printr-un interes insuficient pentru relațiile cu oamenii. Simptomele negative duc adesea la o motivație slabă și la o scădere a scopului comportamentului.
Deficitele cognitive includ probleme de atenție, procesare a limbajului, memorie de lucru, gândire abstractă, rezolvare a problemelor și înțelegere a interacțiunilor sociale. Gândirea pacientului poate deveni rigidă, iar capacitatea de a rezolva probleme, de a înțelege punctele de vedere ale altor persoane și de a învăța din experiență este redusă. Simptomele schizofreniei afectează de obicei capacitatea de a funcționa și interferează semnificativ cu munca, relațiile sociale și îngrijirea de sine. Șomajul, izolarea, relațiile perturbate și scăderea calității vieții sunt frecvente. Severitatea deficienței cognitive determină în mare măsură gradul de dizabilitate generală.
Sinucideri
Cercetările sugerează că cel puțin 5-13% dintre pacienții cu schizofrenie mor prin suicid. [ 66 ] Sinuciderea este principala cauză de deces prematur în rândul persoanelor cu schizofrenie, ceea ce poate explica parțial de ce speranța de viață este redusă în medie cu 10 ani în rândul persoanelor cu schizofrenie. Pacienții cu schizofrenie paranoidă, debut tardiv și funcționare adecvată înainte de boală, care au cel mai bun prognostic pentru recuperare, sunt, de asemenea, mai predispuși să se sinucidă. Deoarece acești pacienți își păstrează capacitatea de a simți durere și suferință, este posibil să fie mai predispuși să acționeze în disperare, pe baza unei înțelegeri realiste a consecințelor bolii lor.
Violenţă
Schizofrenia este un factor de risc relativ minor pentru comportamentul violent. Amenințările cu violența și izbucnirile agresive minore sunt mult mai frecvente decât comportamentele cu adevărat periculoase. Pacienții care sunt mai predispuși să comită acte violente includ cei care abuzează de droguri și alcool, au iluzii de persecuție sau comandă halucinații și cei care nu urmează tratamentul prescris. Foarte rar, pacienții paranoici sever deprimați care se simt izolați îi vor ataca sau ucide pe cei pe care îi percep ca fiind singura sursă a problemelor lor (de exemplu, o figură autoritară, o celebritate, un soț/o soție). Majoritatea pacienților cu schizofrenie nu vor fi niciodată violenți. Pentru fiecare persoană cu schizofrenie care comite o omucidere, 100 se sinucid. [ 67 ] Pacienții cu schizofrenie se pot prezenta la departamentele de urgență cu amenințări cu violența sau pentru a obține hrană, adăpost și îngrijirea necesară.
Etape
Tipuri de progresie a bolii:
- Schizofrenie cronică, continuă și progresivă;
- Schizofrenia paroxistică, care la rândul ei are subtipuri
- Asemănător blănii (paroxistic - progresiv);
- Recurent (periodic).
Stadiile schizofreniei:
- Inițială. De obicei, începe cu astenie, apatie și se manifestă prin depresie profundă, psihoză, delir, hipomanie.
- Manifestare. Simptomele se intensifică, tabloul clinic se blochează și devine fix.
- Etapa finală, ultima. Simptomele sunt de obicei deficitare, tabloul clinic se blochează.
Gradul de viteză (progresivitate) al dezvoltării bolii:
- Schizofrenie malignă (rapid progresivă);
- Schizofrenie paranoidă (moderat progresivă);
- Formă lentă (scăzut progresivă).
Formulare
Au fost descrise cinci forme de schizofrenie: paranoidă, dezorganizată, catatonică, reziduală și nediferențiată. Schizofrenia paranoidă este caracterizată prin idei delirante și halucinații auditive cu funcționare cognitivă și afect intacte. Schizofrenia dezorganizată este caracterizată prin dezorganizarea vorbirii și a comportamentului și afect aplatizat sau inadecvat. În schizofrenia catatonică, predomină simptomele fizice, inclusiv fie imobilitate, fie activitate motorie excesivă și adoptarea unor posturi bizare. În schizofrenia nediferențiată, simptomele sunt mixte. În schizofrenia reziduală, există o dovadă anamnestică clară a schizofreniei cu simptome mai pronunțate, urmată de o perioadă lungă de simptome negative moderat exprimate.
Unii experți, dimpotrivă, clasifică schizofrenia în subtipuri cu deficit și fără deficit, pe baza prezenței și severității simptomelor negative, cum ar fi afectul aplatizat, motivația insuficientă și orientarea scăzută spre scop. Pacienții cu subtipul cu deficit sunt dominați de simptome negative, fără a se lua în considerare alți factori (de exemplu, depresia, anxietatea, stimularea insuficientă a mediului, efectele secundare ale medicamentelor). Pacienții cu subtipul fără deficit pot avea iluzii, halucinații și tulburări de gândire, dar practic nu au simptome negative.
Diagnostice schizofrenii
Nu există teste specifice pentru diagnosticarea schizofreniei. Diagnosticul se bazează pe o evaluare cuprinzătoare a istoricului, simptomelor și semnelor pacientului. [ 76 ] Informațiile din surse suplimentare, cum ar fi familia, prietenii, profesorii și colegii, sunt adesea utile. Conform Manualului de diagnostic și statistic al tulburărilor mintale, ediția a patra (DSM-IV), diagnosticul necesită prezența a două sau mai multe simptome caracteristice (idei delirante, halucinații, vorbire dezorganizată, comportament dezorganizat, simptome negative) pentru o porțiune semnificativă a timpului pe parcursul unei luni, simptomele prodromale ale bolii sau microsimptomele cu deficiențe sociale, ocupaționale și de autoîngrijire trebuie să fie evidente pentru o perioadă de 6 luni, inclusiv 1 lună de simptome evidente.
Psihoza datorată altor afecțiuni medicale sau abuzului de substanțe trebuie exclusă prin examinarea istoricului pacientului și a testelor efectuate, inclusiv teste de laborator și neuroimagistică. Deși la unii pacienți cu schizofrenie se găsesc anomalii cerebrale structurale, acestea nu sunt suficient de specifice pentru a fi diagnostice.
Alte tulburări mintale cu simptome similare includ unele tulburări legate de schizofrenie: tulburarea psihotică tranzitorie, tulburarea schizofreniformă, tulburarea schizoafectivă și tulburarea delirantă. În plus, tulburările de dispoziție pot provoca psihoză la unele persoane. Unele tulburări de personalitate (în special schizoidă) se prezintă cu simptome similare schizofreniei, deși sunt de obicei mai ușoare și nu psihotice.
Când se dezvoltă psihoza, primul pas este încercarea de a-i stabili cauza. Dacă cauza este cunoscută, atunci tratamentul și prevenția pot fi mai specifice. Faptul că un diagnostic precis este cheia unei terapii eficiente poate fi observat în exemplul simptomelor delirante, care pot fi o manifestare nu numai a schizofreniei, ci și a epilepsiei temporale, a dependenței de amfetamine și a fazei maniacale a tulburării afective. Fiecare dintre aceste cazuri necesită un tratament special.
Diagnostic diferentiat
Algoritmul pentru diagnosticul diferențial al schizofreniei poate fi găsit în a 4-a revizie a Manualului de Diagnostic și Statistică a Tulburărilor Mentale al Asociației Americane de Psihiatrie (DSM-IV). Conform acestui algoritm, la un pacient cu psihoză, trebuie excluse mai întâi bolile somatice și abuzul de substanțe. Apoi, trebuie stabilit dacă simptomele sunt cauzate de o tulburare afectivă. Dacă nu, atunci, în funcție de tabloul clinic, se pune diagnosticul de schizofrenie sau tulburare schizotipală. Deși tratamentul tulburărilor psihotice de diverse origini are propriile caracteristici, în toate cazurile, de regulă, se utilizează neuroleptice.
 [ 81 ], [ 82 ], [ 83 ], [ 84 ], [ 85 ], [ 86 ], [ 87 ], [ 88 ], [ 89 ], [ 90 ]
[ 81 ], [ 82 ], [ 83 ], [ 84 ], [ 85 ], [ 86 ], [ 87 ], [ 88 ], [ 89 ], [ 90 ]
Cine să contactați?
Tratament schizofrenii
Schizofrenia este cu siguranță o afecțiune care necesită trimitere la tratament psihiatric. Și aici nu este deloc necesar să existe o legătură directă între experiențele psihotice și infracțiunea comisă. Este suficient ca subiectul să fie bolnav. În general, așa cum confirmă practica, dacă infracțiunea nu este asociată cu simptome psihotice pozitive, atunci este asociată cu o scădere a personalității pacientului ca urmare a bolii. În același timp, desigur, se pot întâlni persoane a căror infracțiune face parte din tiparul lor infracțional de viață și care - s-a întâmplat - s-au îmbolnăvit de schizofrenie, dar, în general, persoanelor care au nevoie în prezent de tratament psihiatric ar trebui să li se ofere un astfel de tratament. Acest lucru nu se întâmplă întotdeauna, mai ales în absența unor servicii de spitalizare satisfăcătoare. Dacă, pe de o parte, subiectul comite o infracțiune în timp ce se află în remisie completă, iar aceasta face parte din „cariera” sa infracțională, atunci el este responsabil pentru acțiunile sale. Schizofrenia poate fi atât de gravă încât subiectul poate fi recunoscut ca incompetent să participe la proces. Această boală stă la baza reducerii răspunderii în cazurile de omor și poate fi baza pentru aplicarea Regulilor MacNaughten.
Timpul scurs de la debutul simptomelor psihotice până la începerea tratamentului se corelează cu rapiditatea răspunsului terapeutic inițial, calitatea răspunsului terapeutic și severitatea simptomelor negative. Tratamentul precoce are ca rezultat, de obicei, un răspuns mai rapid și mai complet. Dacă nu sunt tratați în timpul primului episod, 70-80% dintre pacienți vor dezvolta un episod ulterior în decurs de 12 luni. Utilizarea pe termen lung a antipsihoticelor poate reduce rata de recidivă cu aproximativ 30% pe parcursul unui an.
Principalele obiective ale tratamentului sunt reducerea severității simptomelor psihotice, prevenirea exacerbărilor simptomelor și a deficiențelor de funcționare aferente și ajutarea pacientului să funcționeze la cel mai înalt nivel posibil. Antipsihoticele, reabilitarea comunitară și psihoterapia sunt principalele componente ale tratamentului. Având în vedere că schizofrenia este o boală pe termen lung și recurentă, învățarea pacienților în abilități de auto-ajutorare este un obiectiv important al terapiei.
Pe baza afinității pentru receptorii neurotransmițători specifici și a activității, medicamentele sunt împărțite în antipsihotice tipice (neuroleptice) și antipsihotice de a doua generație (AGG). AGG pot avea anumite avantaje, constând într-o eficacitate ușor mai mare (deși pentru unele AGG aceste avantaje sunt controversate) și o probabilitate redusă de apariție a tulburărilor hiperkinetice și a altor efecte secundare.
Tratamentul schizofreniei cu antipsihotice tradiționale
Mecanismul de acțiune al acestor medicamente este legat în principal de blocarea receptorilor dopaminergici D2 ( blocante ale dopaminei-2). Antipsihoticele tradiționale pot fi împărțite în antipsihotice cu potență mare, intermediară și mică. Antipsihoticele cu potență mare au o afinitate mai mare pentru receptorii dopaminergici și o afinitate mai mică pentru receptorii adrenergici și muscarinici. Antipsihoticele cu potență mică, care sunt rar utilizate, au o afinitate mai mică pentru receptorii dopaminergici și o afinitate relativ mai mare pentru receptorii adrenergici, muscarinici și histaminici. Diversele medicamente sunt disponibile sub formă de comprimate, lichide, injecții intramusculare cu acțiune scurtă și lungă. Alegerea medicamentului se bazează în principal pe profilul efectelor secundare, calea de administrare dorită și răspunsul anterior al pacientului la medicament.[ 91 ]
Antipsihoticele tradiționale
Clasă |
Pregătire (limite) |
Doza zilnică |
Doza medie |
Comentarii |
Fenotiazine alifatice |
Clorpromazină |
30-800 |
400 mg pe cale orală la culcare |
Prototip de medicamente cu potență redusă. De asemenea, în supozitoare rectale. |
Piperidină |
Tioridazină |
150-800 |
400 mg pe cale orală la culcare |
Singurul medicament cu o doză maximă absolută (800 mg/zi) - în doze mari provoacă retinopatie pigmentară și are un efect anticolinergic pronunțat. Atenționări suplimentare sunt incluse în instrucțiuni din cauza prelungirii intervalului QTk. |
Dibenzoxazepine |
Loxapină |
20-250 |
60 mg oral la culcare |
Are afinitate pentru receptorii dopaminei D și serotoninei 5HT |
Dihidroindolone |
Molindon |
15-225 |
60 mg oral la culcare |
Poate cauza pierdere în greutate |
Tioxantene |
Tiotixenă |
8-60 |
10 mg oral la culcare |
Incidență ridicată a acatiziei |
Butirofenone |
Haloperidol |
1-15 |
4 mg oral la culcare |
Prototip de medicamente cu potență mare; este disponibil decanoat de haloperidol (i/m depot). Acatizia este frecventă. |
Difenil butilpiridine |
Pimozidă |
1-10 |
3 mg oral la culcare |
Aprobat doar pentru sindromul Tourette |
Piperazină |
Trifluoperazină Flufenazină Perfenazină 2 ' 3 |
2-40 0,5-40 12-64 |
10 mg oral la culcare 7,5 mg oral la culcare 16 mg oral la culcare |
Există, de asemenea, decanoat de flufenazină și enantat de flufenazină, care sunt forme depot (nu există echivalente de doză) |
Interval QTk - 07" corectat pentru ritmul cardiac.
1 Recomandările actuale pentru inițierea tratamentului cu antipsihotice tipice sunt de a începe cu cea mai mică doză și de a crește treptat doza până la doza necesară; se recomandă ora de culcare. Nu există dovezi că creșterea rapidă a dozei este mai eficientă. Sunt disponibile formulări intramusculare pentru tratamentul acut.
Antipsihoticele convenționale au unele efecte secundare grave, inclusiv sedare, confuzie, distonie sau rigiditate musculară, tremor, niveluri crescute de prolactină și creștere în greutate (pentru tratarea efectelor secundare). Acatizia (agitație motorie) este deosebit de supărătoare și poate duce la o respectare deficitară a tratamentului. Aceste medicamente pot provoca, de asemenea, diskinezie tardivă, o tulburare de mișcare involuntară, caracterizată cel mai adesea prin încrețirea buzelor și a limbii și/sau o senzație de „răsucire” a brațelor sau picioarelor. Incidența diskineziei tardive este de aproximativ 5% pe an de utilizare a medicamentelor în rândul pacienților care iau antipsihotice convenționale. În aproximativ 2% din cazuri, diskinezia tardivă este grav desfigurantă. La unii pacienți, diskinezia tardivă persistă pe termen nelimitat, chiar și după oprirea administrării medicamentului.
Două antipsihotice tradiționale și un antipsihotic sunt disponibile sub formă de preparate cu acțiune prelungită, cu efect de depot. Aceste preparate sunt utilizate pentru a evita incompatibilitățile medicamentoase. De asemenea, pot ajuta pacienții care, din cauza dezorganizării, indiferenței sau aversiunii față de boală, nu își pot administra medicamentele pe cale orală zilnic.
Antipsihotice depozitate
Pregătirea 1 |
Dozare |
Timpul până la vârful 2 |
Decanoat de flufenazină |
12,5-50 mg la fiecare 2-4 săptămâni |
1 zi |
Enantatul de flufenazină |
12,5-50 mg la fiecare 1-2 săptămâni |
2 zile |
Decanoat de haloperidol |
25-150 mg la fiecare 28 de zile (posibil la fiecare 3-5 săptămâni) |
7 zile |
Microsfere de risperidonă S |
25-50 mg la fiecare 2 săptămâni |
35 de zile |
1 Administrat intramuscular folosind tehnica Z-track.
2 Timpul până la atingerea nivelului maxim după o singură doză.
Deoarece există o întârziere de 3 săptămâni între prima injecție și atingerea unor concentrații sanguine adecvate, pacientul trebuie să continue terapia antipsihotică orală timp de 3 săptămâni după prima injecție. Se recomandă evaluarea tolerabilității înainte de inițierea tratamentului cu risperidonă orală.
Clozapina este singurul SGA care s-a dovedit a fi eficient la aproximativ 50% dintre pacienții rezistenți la antipsihoticele tradiționale. Clozapina reduce simptomele negative, nu provoacă practic efecte secundare motorii, are un risc minim de a dezvolta diskinezie tardivă, dar provoacă și alte efecte nedorite, cum ar fi sedarea, hipotensiune arterială, tahicardia, creșterea în greutate, diabetul zaharat de tip 2 și creșterea salivației. Clozapina poate provoca, de asemenea, convulsii, acest efect fiind dependent de doză. Cel mai sever efect secundar este agranulocitoza, care se poate dezvolta la aproximativ 1% dintre pacienți. Prin urmare, este necesară monitorizarea frecventă a numărului de leucocite, iar clozapina este de obicei utilizată ca medicament de rezervă la pacienții care nu răspund adecvat la alte medicamente. [ 92 ], [ 93 ]
Noile SGA-uri au multe dintre avantajele clozapinei, fără riscul de agranulocitoză și sunt în general preferate antipsihoticelor tradiționale pentru tratamentul episoadelor acute și prevenirea exacerbărilor. Noile SGA-uri au o eficacitate foarte similară, dar au efecte secundare diferite, astfel încât alegerea medicamentului se bazează pe sensibilitatea individuală și pe alte caracteristici ale medicamentului. De exemplu, olanzapina, care prezintă un risc relativ ridicat la pacienții care primesc terapie de întreținere pe termen lung, trebuie evaluată cel puțin la fiecare 6 luni. Se pot utiliza instrumente de evaluare, cum ar fi Scala Mișcărilor Involuntare Anormale. Sindromul neuroleptic malign este un eveniment advers rar, dar potențial fatal, caracterizat prin rigiditate musculară, febră, instabilitate autonomă și niveluri crescute ale creatinin fosfokinazei.
Aproximativ 30% dintre pacienții cu schizofrenie nu răspund la antipsihoticele tradiționale. În aceste cazuri, clozapina, un antipsihotic de a doua generație, poate fi eficientă.
Tratamentul schizofreniei cu antipsihotice de a doua generație
Antipsihoticele de a doua generație acționează prin blocarea atât a receptorilor dopaminergici, cât și ai serotoninei (antagoniști ai receptorilor serotonină-dopamină). AGV reduc în general simptomele pozitive; pot reduce simptomele negative într-o măsură mai mare decât antipsihoticele tradiționale (deși astfel de diferențe sunt controversate); pot provoca mai puține deficiențe cognitive; sunt mai puțin susceptibile de a provoca efecte secundare extrapiramidale (motorice); prezintă un risc mai mic de a dezvolta diskinezie tardivă; unele AGV nu provoacă sau provoacă doar o ușoară creștere a nivelului de prolactină.
Scala Mișcării Involuntare Patologice
- Observați mersul pacientului în drum spre cabinet.
- Rugați pacientul să îndepărteze guma de mestecat sau protezele dentare dacă acestea cauzează probleme.
- Stabiliți dacă pacientul este conștient de anumite mișcări.
- Puneți pacientul să stea pe un scaun ferm, fără cotiere, cu mâinile în poală, picioarele ușor depărtate și tălpile pe podea. Acum și pe tot parcursul examinării, observați întregul corp al pacientului pentru a evalua mișcarea.
- Instruiți pacientul să stea cu brațele atârnând nesprijinite peste genunchi.
- Rugați pacientul să deschidă gura de două ori. Observați mișcările limbii.
- Rugați pacientul să scoată limba de două ori.
- Rugați pacientul să bată ușor cu degetul mare pe celelalte degete ale mâinii timp de 15 secunde pe fiecare mână. Observați fața și picioarele.
- Rugați pacientul să stea în picioare cu brațele întinse înainte.
Evaluați fiecare element pe o scală de la 0 la 4 în funcție de gradul de creștere a severității. 0 - niciunul; 1 - minim, poate fi limita extremă a normei; 2 - ușor; 3 - moderat; 4 - sever. Dacă mișcările sunt observate numai după activare, acestea trebuie evaluate cu 1 punct mai puțin decât cele care apar spontan.
Mișcări faciale și orale |
Expresii faciale Buze și zona periorală Fălci Limbă |
Mișcări ale membrelor |
Mâini Picioare |
Mișcările trunchiului |
Gât, umeri, șolduri |
Concluzie generală |
Severitatea mișcărilor patologice Eșec datorat mișcărilor patologice Conștientizarea de către pacient a mișcărilor anormale (0 - nu este conștient; 4 - disconfort sever) |
Adaptat după: Manualul de evaluare ECDEU pentru psihofarmacologie de W. Guy. Drepturi de autor 1976 de către Departamentul de Sănătate, Educație și Bunăstare al SUA.
Creșterea în greutate, hiperlipidemia și riscul crescut de diabet zaharat de tip 2 sunt principalele efecte adverse ale inhibitorilor ECA. Prin urmare, înainte de inițierea tratamentului cu inhibitori ECA, toți pacienții trebuie evaluați pentru factorii de risc, inclusiv antecedentele personale/familiale de diabet zaharat, greutatea, circumferința taliei, tensiunea arterială, glicemia à jeun și profilul lipidic. Pacienții și familiile acestora trebuie educați cu privire la semnele și simptomele diabetului (poliurie, polidipsie, pierdere în greutate), inclusiv cetoacidoza diabetică (greață, vărsături, deshidratare, respirație rapidă, vedere încețoșată). În plus, toți pacienții care încep tratamentul cu inhibitori ECA trebuie consiliați cu privire la nutriție și activitate fizică. Toți pacienții tratați cu antipsihotice necesită monitorizare periodică a greutății corporale, a indicelui de masă corporală (IMC), a glicemiei à jeun și trebuie trimiși la o evaluare specială dacă apare hiperlipidemie sau diabet zaharat de tip 2. Sindromul neuroleptic malign a fost asociat cu practic toate medicamentele antipsihotice, inclusiv cu neurolepticele nou comercializate.[ 94 ]
Antipsihotice de a doua generație 1
FATĂ |
Pregătire |
Limite de doză |
Doza medie pentru adulți |
Comentarii |
Dibenzodiazepine |
Clozapină |
150-450 mg oral de 2 ori pe zi |
400 mg pe cale orală la culcare |
Primul AAS care a demonstrat eficacitate la pacienții rezistenți la tratament. Necesită monitorizarea frecventă a numărului de leucocite din cauza riscului de agranulocitoză; crește riscul de convulsii, creștere în greutate. |
Benzoxazoli |
Risperidonă |
4-10 mg oral înainte de culcare |
4 mg oral la culcare |
Poate provoca simptome extrapiramidale la doze >6 mg; creștere dependentă de doză a nivelului de prolactină; singurul AINS cu formă injectabilă cu acțiune prelungită |
Tienobenzodiazepine |
Olanzapină |
10-20 mg oral înainte de |
15 mg oral la culcare |
Somnolența, creșterea în greutate și amețelile sunt cele mai frecvente reacții adverse. |
Dibenzotiazepine |
Quetiapină |
150-375 mg oral de 2 ori pe zi |
200 mg oral de 2 ori pe zi |
Potența scăzută permite o dozare largă; nu există efect anticolinergic. Ajustarea treptată a dozei este necesară din cauza blocării receptorilor α; este necesară administrarea de două ori pe zi. |
Benzizotiazolilpiperazine |
Ziprasidonă |
40-80 mg oral de 2 ori pe zi |
80 mg oral de 2 ori pe zi |
Inhibă recaptarea serotoninei și norepinefrinei, poate avea proprietăți antidepresive. Cel mai scurt timp de înjumătățire al medicamentelor noi; necesită administrare de două ori pe zi, cu alimente. Pentru afecțiuni acute, este disponibilă o formă intramusculară. Tendință scăzută de creștere a greutății corporale. |
Dihidrocarostiril |
Aripiprazol |
10-30 mg oral înainte de |
15 mg oral la culcare |
Agonist parțial al receptorilor dopaminergici-2, tendință scăzută la creștere în greutate |
APVP-urile sunt antipsihotice de a doua generație.
1 Monitorizarea creșterii în greutate și a dezvoltării diabetului de tip 2 este recomandată pentru această clasă de antipsihotice.
Toate antipsihoticele de a doua generație sunt asociate cu o mortalitate crescută la pacienții vârstnici cu demență.
Tratamentul schizofreniei cu neuroleptice atipice a început aproape simultan cu începerea prescrierii neurolepticelor tipice pacienților cu schizofrenie.
Servicii de reabilitare și asistență socială
Programele de formare în abilități psihosociale și de reabilitare profesională îi ajută pe mulți pacienți să lucreze, să facă cumpărături și să aibă grijă de ei înșiși, să își gestioneze gospodăria, să se înțeleagă cu ceilalți și să colaboreze cu profesioniști din domeniul sănătății mintale. Menținerea locului de muncă poate fi deosebit de valoroasă atunci când pacientul este plasat într-un mediu de lucru competitiv și i se oferă un mentor la locul de muncă pentru a facilita adaptarea la muncă. În timp, mentorul la locul de muncă acționează doar ca o rezervă pentru luarea deciziilor sau pentru comunicarea cu angajatorii.
Serviciile de sprijin comunitare permit multor persoane cu schizofrenie să trăiască în comunitate. Deși majoritatea pacienților pot trăi independent, unii necesită locuințe supravegheate, unde personalul este prezent pentru a asigura respectarea medicației. Programele oferă niveluri gradate de supraveghere într-o varietate de contexte, de la sprijin 24 de ore din 24 până la vizite periodice la domiciliu. Aceste programe ajută la asigurarea autonomiei pacientului, în timp ce furnizarea de îngrijiri medicale adecvate reduce probabilitatea recidivelor și necesitatea spitalizării. Programele de tratament comunitare funcționează la domiciliul pacientului sau în altă locație și au raporturi ridicate personal-pacienți; echipele de tratament furnizează direct cea mai mare parte sau tot tratamentul necesar.
În timpul exacerbărilor severe, poate fi necesară spitalizarea sau intervenția de criză într-un spital, precum și spitalizarea involuntară dacă pacientul reprezintă un pericol pentru sine sau pentru ceilalți. În ciuda unor servicii de reabilitare și sociale mai bune, un număr mic de pacienți, în special cei cu deficite cognitive severe și cei rezistenți la tratament, necesită spitalizare pe termen lung sau alte îngrijiri de susținere.
Psihoterapie
Modelele actuale de psihoterapie pentru schizofrenie, temperate în mare măsură de eforturile anterioare dezamăgitoare, sunt mai modeste și pragmatice în obiectivele lor și sunt văzute ca parte a unui tratament cuprinzător, cu intervenții farmacologice în centrul lor. [ 95 ] Scopul psihoterapiei este de a dezvolta o relație integrată între pacient, familie și medic, astfel încât pacientul să poată învăța să înțeleagă și să gestioneze boala sa, să ia medicamentele conform prescripției și să facă față stresului mai eficient. Deși o abordare comună este combinarea psihoterapiei individuale cu medicația, există puține îndrumări practice în acest sens. Cea mai eficientă psihoterapie este cea care începe prin abordarea nevoilor sociale de bază ale pacientului, oferă sprijin și educație cu privire la natura bolii, promovează funcționarea adaptivă și se bazează pe empatie și o înțelegere dinamică adecvată a schizofreniei. Mulți pacienți necesită sprijin psihologic empatic pentru a se adapta la faptul că boala este adesea o tulburare pe tot parcursul vieții, care poate limita semnificativ funcționarea.
Pentru pacienții care locuiesc cu familiile lor, intervențiile psihoeducaționale familiale pot reduce ratele de recidivă. Grupurile de sprijin și advocacy, cum ar fi Alianța Națională pentru Bolnavii Mintali, sunt adesea utile familiilor.
Mai multe informații despre tratament
Prognoză
În primii 5 ani de la debutul bolii, funcționarea poate fi afectată, abilitățile sociale și profesionale pot scădea, iar neglijarea îngrijirii de sine poate crește progresiv. Simptomele negative pot crește în severitate, iar funcționarea cognitivă poate scădea. Ulterior, deficiențele ating un platou. Există unele dovezi că severitatea bolii poate scădea odată cu vârsta, în special la femei. Tulburările hiperkinetice se pot dezvolta la pacienții cu simptome negative severe și disfuncție cognitivă, chiar dacă nu se utilizează antipsihotice.
Prognosticul variază în funcție de forma de schizofrenie. Pacienții cu schizofrenie paranoidă au o dizabilitate mai mică și răspund mai bine la tratament. Pacienții cu subtipul deficitar sunt de obicei mai dizabili, au un prognostic mai slab și sunt mai rezistenți la terapie.
Schizofrenia poate fi asociată cu alte tulburări mintale. [ 96 ] Dacă este asociată cu simptome obsesiv-compulsive, prognosticul este deosebit de slab; dacă este asociată cu simptome de tulburare de personalitate borderline, prognosticul este mai bun. Aproximativ 80% dintre persoanele cu schizofrenie experimentează unul sau mai multe episoade de depresie majoră la un moment dat în viață.
În primul an după diagnosticare, prognosticul este strâns legat de respectarea strictă a medicației psihotrope prescrise. În general, 1/3 dintre pacienți obțin o ameliorare semnificativă și durabilă; 1/3 prezintă o oarecare ameliorare, dar au exacerbări periodice și afectare reziduală; 1/3 au simptome severe și persistente. Doar 15% dintre toți pacienții revin complet la nivelul de funcționare de dinainte de boală. Factorii asociați cu un prognostic bun includ o funcționare bună de dinainte de boală (de exemplu, performanțe academice bune, succes la locul de muncă), debutul tardiv și/sau brusc al bolii, antecedente familiale de tulburări de dispoziție, altele decât schizofrenia, afectare cognitivă minimă, simptome negative ușoare și formă paranoidă sau fără deficit. Factorii asociați cu un prognostic slab includ vârsta precoce de debut, funcționarea deficitară de dinainte de boală, antecedentele familiale de schizofrenie și subtipul dezorganizat sau deficitar cu simptome negative multiple. Bărbații au rezultate mai slabe decât femeile; femeile răspund mai bine la terapia antipsihotică.
Abuzul de alcool și droguri reprezintă probleme semnificative la aproximativ 50% dintre persoanele cu schizofrenie. Dovezile anecdotice sugerează că marijuana și alte halucinogene pot fi extrem de distructive la persoanele cu schizofrenie și ar trebui descurajate. Abuzul concomitent de substanțe este un predictor puternic al unui prognostic nefavorabil și poate duce la nerespectarea medicației, recidive, spitalizări frecvente, funcționare scăzută și pierderea sprijinului social, inclusiv lipsa de adăpost.

