
Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Rolul modificărilor în osul subcondral în patogeneza osteoartritei
Expert medical al articolului
Ultima examinare: 04.07.2025
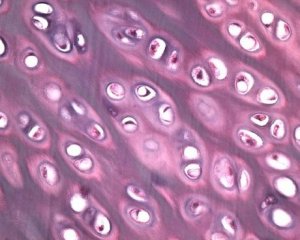
Odată cu degenerarea cartilajului articular, țesutul osos subiacent este, de asemenea, implicat în procesul patologic al osteoartrozei. Se presupune că îngroșarea plăcii subcondrale contribuie la progresia osteoartrozei. Pe măsură ce osteoartroza progresează, cartilajul articular, care este supus stresului mecanic și chimic, se erodează lent din cauza unui dezechilibru în procesele de catabolism și reparare a cartilajului. În special, stresul mecanic în raport cu articulațiile care „suportă” greutatea corporală contribuie la formarea unui număr mare de microfracturi în placa subcondrală și în cartilaj. Pe măsură ce cartilajul articular se erodează, scleroza osului subcondral progresează, rigiditatea țesutului osos crește, ceea ce, la rândul său, contribuie la perturbarea suplimentară a structurii cartilajului articular. Cu toate acestea, problema naturii primare sau secundare a modificărilor osoase subcondrale în osteoartroză rămâne nerezolvată.
Până de curând, modificările detectabile radiografic ale substanței spongioase a osului subcondral, cum ar fi scleroza sau formarea de chisturi, erau considerate secundare la pacienții cu osteoartroză. Cu toate acestea, rezultatele studiilor clinice și experimentale indică un posibil rol inițiator al osului subcondral în patogeneza osteoartrozei. Unul dintre mecanismele posibile este o creștere bruscă a gradientului de rigiditate al osului subcondral, datorită faptului că integritatea țesutului cartilajului subiacent depinde de proprietățile mecanice ale „patului” său osos. Studiile efectuate pe primate au arătat că modificările osului subcondral pot preceda modificările cartilajului articular. Dovezile pro și contra acestei ipoteze, apărute ca urmare a studiilor pe modele animale de osteoartroză și a studiilor clinice, nu au făcut decât să intensifice dezbaterea. Îngroșarea trabeculelor din osul subcondral nu este întotdeauna însoțită de o creștere a mineralizării osoase sau, mai degrabă, de o creștere a volumului osteoidului. Acest semn de mineralizare anormală indică faptul că perturbarea reglării remodelării osoase este o parte integrantă a osteoartritei și susține, de asemenea, conceptul de defect al celulelor osoase în osteoartrite. Grupul lui J. Dequeker (1989) consideră că aceasta din urmă este o „boală metabolică osoasă generalizată”.
Țesutul osos este reînnoit constant. Acest proces dinamic, numit remodelare osoasă, este o secvență complexă de resorbție și mineralizare. Osteoclastele resorb țesutul osos, iar osteoblastele secretă proteine care formează principala componentă organică pentru mineralizare. Formarea și resorbția osoasă nu apar aleatoriu în întregul schelet; este un proces programat care are loc în diferite zone ale scheletului, numite unități de remodelare osoasă. La începutul ciclului, osteoclastele apar pe suprafața inactivă; în decurs de 2 săptămâni, acestea formează un tunel în osul cortical sau o lacună pe suprafața osului trabecular. Frecvența activării noilor unități de remodelare osoasă determină gradul de reînnoire osoasă. La o persoană tânără sănătoasă, procesele de formare și resorbție osoasă sunt echilibrate, iar masa osoasă normală este menținută. În reglarea hormonală a resorbției țesutului osos, participă cel puțin PTH și PGE2 , nu numai osteoclastele, ci și osteoblastele, deoarece sub influența acestor hormoni, sunt eliberați factori care stimulează resorbția osoasă de către osteoclaste. În prezent, sunt cunoscuți peste 12 regulatori locali și sistemici ai creșterii țesutului osos care afectează remodelarea acestuia, în special PTH, 1,25(OH)2D3 ,calcitonina, hormonul de creștere, glucocorticoizii, hormonii tiroidieni, insulina, IGF (1 și 2), estrogenii, PGE2 , androgenii.
Celulele osoase eliberează o serie de proteine și citokine care efectuează reglarea endocrină și transducția semnalului. Proteinele produse de osteoblaste includ proteine ale matricei osoase, cum ar fi colagenul, osteopontina, osteocalcina, sialoproteinele osoase. În plus, aceste celule eliberează proteaze atât în forme active, cât și latente, care participă la procesul de remodelare a țesutului osos - MMP-uri, componente ale sistemului activator de plasminogen (PA)/plasmină. Citokinele eliberate de osteoblaste pot acționa atât prin mecanisme autocrine, cât și prin căi paracrine asupra celulelor locale (alte osteoblaste, osteoclaste).
Nu se știe încă dacă aceste semnale sunt reglate de stresul mecanic sau de alte semnale chimice induse de stresul mecanic. Cu toate acestea, se știe că stresul mecanic repetat provoacă proliferarea locală a celulelor osoase și/sau a proteinelor. In vivo, încărcarea mecanică poate activa osteoblastele, poate crește nivelul nucleotidelor ciclice, producția de prostaglandine și poate provoca modificări morfologice asociate cu remodelarea osoasă. In vitro, stresul mecanic provoacă proliferarea culturilor de osteoblaste, exprimarea ARNm a proteinelor osoase implicate în formarea și mineralizarea osteoidului, eliberarea factorilor de creștere locali, cum ar fi IGF-1 și IGF-2, și a moleculelor de adeziune. Transmiterea semnalului de stres mecanic se poate realiza prin canale ionice mecanosensibile.
Există dovezi indirecte ale disfuncției osteoblastelor în osteoartroză. G. Gevers și J. Dequeker (1987) au demonstrat o creștere a nivelului seric de osteocalcină la femeile cu osteoartroză la nivelul mâinii, precum și în explantele osoase corticale, indicând faptul că patologia osoasă poate face parte din osteoartroză. Autopsia a relevat nu numai o îngroșare a osului subcondral, ci și o mineralizare anormal de scăzută a capului femural. La cobaii cu osteoartroză indusă chirurgical, tomografia computerizată a evidențiat o îngroșare semnificativă a fracției osoase în zona subcondrală. Un dezechilibru între proteinele colagene și cele non-colagene (osteocalcină etc.) poate duce la o creștere a volumului osos, dar nu afectează densitatea sa minerală. Conform lui M. Shimizu și colab. (1993), progresia modificărilor degenerative ale cartilajului articular este asociată cu o remodelare mai intensivă a osului subcondral și o creștere a rigidității acestuia, ceea ce indică, de asemenea, un defect al celulelor țesutului osos în osteoartroză. Conform ipotezei propuse de B. Lee și M. Aspden (1997), proliferarea celulelor osoase defecte poate duce la o creștere a rigidității țesutului osos, dar nu provoacă o creștere a densității sale minerale.
CI Westacott și colab. (1997) au emis ipoteza că osteoblastele anormale afectează direct metabolismul cartilajului. Cultivând osteoblaste de la pacienți cu osteoartrită cu condrocite de la persoane care nu aveau afecțiuni articulare, autorii au observat o modificare semnificativă a eliberării de glicozaminoglicani de către țesutul cartilajului normal in vitro, dar nivelul eliberării de citokine a rămas neschimbat. G. Hilal și colab. (1998) au arătat că cultura de osteoblaste din osul subcondral al pacienților cu osteoartrită in vitro prezintă un metabolism alterat - activitatea sistemului AP/plasmină și nivelul de IGF-1 din aceste celule sunt crescute. Observația lui CI Westacott și colab. (1997) poate fi explicată printr-o creștere a activității proteazelor în celulele osoase subcondrale.
Rămâne necunoscut dacă modificările osului subcondral inițiază osteoartrita sau contribuie la progresia acesteia. DK Dedrick și colab. (1993) au demonstrat că la câinii cu osteoartrita indusă chirurgical, îngroșarea osului subcondral nu este o condiție necesară pentru dezvoltarea modificărilor asemănătoare osteoartrozei în cartilajul articular, dar contribuie la progresia proceselor degenerative din cartilaj. Rezultatele studiului realizat de A. Sa'ied și colab. (1997) contrazic datele studiului anterior. Folosind ecografia de 50 MHz pentru a evalua modificările morfologice inițiale și progresia acestora în cartilajul articular și os în osteoartrita experimentală indusă prin injecții de acid monoiodoacetic în articulația sufixului la șobolani, autorii au demonstrat un proces simultan de modificări ale osului și cartilajului în primele trei zile după injecție.
Osteoblastele secretă factori de creștere și citokine implicate în remodelarea osoasă locală, care pot promova remodelarea cartilajului propriu-zis în articulațiile „purtătoare de greutate” după penetrarea lor prin microfisuri în stratul calcificat al cartilajului articular. Mai mult, produșii secretori ai celulelor osoase se găsesc în lichidul sinovial. Cele mai probabile produse secretate de osteoblastele anormale care pot iniția procesul de remodelare locală a cartilajului sunt TGF-β și proteinele morfometrice osoase (BMP). Ambii membri ai familiei TGF sunt secretați atât de condrocite, cât și de osteoblaste și ambii sunt capabili să modifice atât remodelarea osoasă, cât și cea a cartilajului. J. Martel Pelletier și colab. (1997) au observat o creștere a nivelului de TGF-β în explantele osoase subcondrale ale pacienților cu osteoartroză în comparație cu indivizii sănătoși, ceea ce indică un rol probabil al acestui factor de creștere în patogeneza osteoartrozei. IGF-urile sunt, de asemenea, produse de osteoblaste. Într-o cultură de celule asemănătoare osteoblastelor obținute de la pacienți cu osteoartroză, s-a constatat o creștere a nivelului de IGF-uri, care alterează metabolismul cartilajului.
TGF-b, IGF, BMP și citokinele produse de osteoblaste în osul subcondral pot influența producția de colagenază și alte enzime proteolitice din cartilaj, ceea ce, la rândul său, poate promova remodelarea/degradarea matricei cartilajului. Rămâne neclar dacă osteoblastele din OA produc mai puțin factor de stimulare a coloniilor de macrofage (M-CSF - un stimulator al resorbției osoase) decât celulele normale. Rezultatele studiilor realizate de AG Uitterlinden și colab. (1997) au arătat că receptorii vitaminei D, care sunt exprimați de osteoblaste și reglează expresia unui număr de factori sintetizați de aceste celule, pot juca un anumit rol în formarea osteofitelor, ceea ce explică parțial rolul osteoblastelor în patogeneza acestei boli.
Luând în considerare rezultatele studiilor menționate mai sus, G. Hilal și colab. (1998), J. Martel-Pelletier și colab. (1997) au propus următoarea ipoteză de lucru privind relația dintre remodelarea osoasă subcondrală și cartilajul articular corespunzător în osteoartroză. Într-un stadiu incipient sau avansat al patogenezei OA, procesul de remodelare a țesutului osos din osul subcondral se intensifică. În același timp, încărcarea repetată duce la microfracturi locale și/sau apariția unui dezechilibru în sistemul IGF/proteină de legare a IGF (IGFBP) din cauza unui răspuns anormal al osteoblastelor osoase subcondrale, ceea ce contribuie la scleroza acestuia. Acestea din urmă, la rândul lor, pot contribui la apariția microfracturilor cartilajului propriu și la deteriorarea matricei acestuia.
În condiții normale, această leziune este reparată prin sinteza locală și eliberarea de IGF-1 și proteine care leagă IGF, care stimulează formarea ECM a cartilajului articular. În același timp, sistemul GF promovează creșterea celulelor osoase subcondrale și formarea matricei osoase. Activitatea anabolică a sistemului IGF este crescută în osul subcondral al pacienților cu osteoartroză, în timp ce activarea locală a sistemului AP/plasmină (un regulator local al sistemului IGF) în cartilajul articular provoacă modificări locale ale acestuia. În osteoblastele cu osteoartroză, IGF-1 perturbă reglarea AP de către plasmină prin feedback pozitiv, prin urmare, poate restricționa remodelarea în țesutul osos, ceea ce duce în cele din urmă la scleroză subcondrală. Astfel, în țesutul osos și cartilaj, inducerea locală a IGF-1 și a proteazelor duce, pe de o parte, la deteriorarea cartilajului, pe de altă parte, la îngroșarea osului subcondral, acesta din urmă contribuind la deteriorarea suplimentară a cartilajului. Dezechilibrul dintre deteriorarea cartilajului asociată cu scleroza subcondrală și capacitățile sale reparative duce la modificări progresive ale matricii extracelulare (ECM) a cartilajului și la dezvoltarea osteoartrozei. Potrivit autorilor, această ipoteză explică și progresia lentă a bolii.

