
Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Restenoza
Expert medical al articolului
Ultima examinare: 04.07.2025
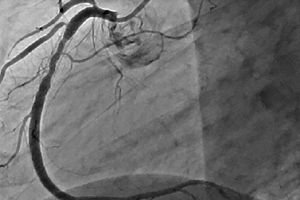
Restenoza este dezvoltarea unei îngustări recurente de 50% sau mai mult la locul intervenției coronariene percutanate. Restenoza este de obicei însoțită de angină pectorală recurentă, care necesită adesea intervenții repetate. Pe măsură ce intervenția coronariană percutanată a evoluat, incidența restenozei a scăzut, iar natura acesteia s-a schimbat și ea.
Restenoză după angioplastie coronariană transluminală cu balon (TBCA)
După angioplastia totală de sânge (TBCA), rata restenozei în primele 6 luni este de 30-40%. Principalul mecanism al dezvoltării acesteia este remodelarea locală negativă a vasului, care, în esență, este un colaps elastic al lumenului arterial, dilatat de balon în timpul procedurii. Formarea locală de trombi și creșterea neointimală joacă, de asemenea, un rol relativ. Există factori de risc clinici (diabet zaharat de tip 2, sindrom coronarian acut (SCA), antecedente de restenoză), angiografici (leziune a arterei laterale laterale (LAD), diametru mic al vasului, ocluzie totală cronică (CTO), leziune lungă, grefe de bypass venoase degenerate) și procedurali (stenoză reziduală mare, creștere mică a diametrului vasului ca urmare a umflării balonului) pentru restenoză după TBCA. În caz de restenoză, de obicei se efectuează o intervenție repetată. Succesul TBCA repetate la locul restenozei este comparabil cu prima procedură. Cu toate acestea, cu fiecare TBCA ulterioară pentru restenoză, riscul de restenoză recurentă crește semnificativ. După a 3-a încercare, acesta ajunge la 50-53%. În plus, cu fiecare angiografie coronariană completă (TBCA), restenoza care se dezvoltă este mai pronunțată decât prima. Factorii de risc pentru restenoză după a doua TBCA sunt apariția precoce a primei restenoze (60-90 de zile după procedură), afectarea diafragmei laterale (LAD), afectarea multivasculară, diabetul zaharat de tip 2, hipertensiunea arterială, angina pectorală instabilă și umflarea multiplă a balonului în timpul primei proceduri. Având în vedere frecvența ridicată a restenozei și mecanismul de dezvoltare a acesteia, în practica clinică au fost introduse stenturile coronariene, care teoretic ar fi trebuit să elimine remodelarea negativă a vaselor după TBCA.
Primele studii care au demonstrat eficacitatea stentării au fost studiile STRESS și BENESTENT publicate în 1993. BENESTENT a inclus 516 pacienți cu stenoză nou diagnosticată la nivelul arterelor coronare cu diametrul mai mare de 3 mm, care au fost randomizați în două grupuri: angiografie coronară completă (TBCA) convențională (n = 257) și TBCA cu plasare de stent (n = 259). După 3 ani, rata de restenoză în timpul angiografiei a fost de 32% în grupul cu TBCA convențională și de 22% în grupul cu stent. Reducerea relativă a ratei de restenoză a fost de 31% (p < 0,01). Grupul cu stent a avut, de asemenea, o nevoie mai mică de revascularizare miocardică repetată (10% vs. 20,6% în grupul cu TBCA convențională; p < 0,01), ceea ce a fost asociat cu o rată mai mică de recurență a anginei pectoris în grupul cu stent.
Conform studiului STRESS (n = 407), rata restenozei a fost, de asemenea, mai mică în grupul cu stentare (n ~ 205) decât în grupul cu angioplastie transtomografică percutanată (PTCA) convențională (n = 202) - 31,6 vs. 42,1% (p < 0,01). Avantajul utilizării stentului față de angioplastia convențională în cazul restenozei la locul PTCA a fost demonstrat în studiul REST, în care 383 de pacienți cu restenoză au fost randomizați pentru stentare sau angioplastie coronariană transluminală percutanată repetată. Restenoza repetată detectată angiografic a fost cu 18% mai mică în grupul cu stentare (18 vs. 5,32%; p < 0,03). Revascularizarea miocardică repetată, care este un indicator al restenozei semnificative clinic, a fost, de asemenea, necesară semnificativ mai puțin frecvent în grupul de pacienți care au suferit stentare (10 vs. 27%; p < 0,001). Astfel, s-au dovedit rezultate mai bune cu utilizarea stentului nu numai în arterele native, ci și în cazul intervenției pentru restenoză dezvoltată după TBCA.
Restenoză după implantarea de stent gol (BSI)
Deși stenturile coronariene neacoperite au redus incidența restenozei cu 30-40% în comparație cu angiografia coronariană totală (TBCA), 17-32% dintre pacienți dezvoltă restenoză în stent chiar și după stentare, necesitând revascularizare repetată. Mecanismul dezvoltării stenozei în stent (ISS) diferă de cel din TBCA. După stentare, principala contribuție la restenoză este formarea neointimei, mai degrabă decât remodelarea negativă, ca în TBCA, care este practic absentă la locul implantării stentului. Neointimă se formează prin migrarea și proliferarea celulelor musculare netede care produc matricea extracelulară, care împreună cu celulele alcătuiește neointimă. În plus, persistența trombusului la locul stentării este, de asemenea, importantă la pacienții cu diabet zaharat.
Principala clasificare a stenozei intra-stent (ISS) este cea propusă de Mehran, care include patru tipuri în funcție de extinderea și severitatea leziunii: ISS de tip I - locală (< 10 mm lungime), tip II - difuză (> 10 mm lungime), tip III - proliferativă (> 10 mm și care se extinde dincolo de stent) și tip IV - ISS care duce la ocluzie. Primul tip este împărțit în subtipuri în funcție de localizarea în stent: 1a - pe curbă sau între stenturi, 1b - marginală, 1c - în interiorul stentului, 1d - multifocală.
Factorii de risc pentru dezvoltarea restenozei stentului marginal (VRS) sunt intervențiile pe bypass venos, ocluziile cronice, leziunile ostiale, diametrul mic al vasului, prezența stenozei reziduale, stentarea pentru VRS, diametrul mic al vasului post-procedural, leziunea diafragmei laterale (LAD), lungimea mare a stentului, prezența diabetului zaharat, implantarea mai multor stenturi într-o singură leziune. Există indicii ale influenței factorilor genetici, în special polimorfismul genei glicoproteinei IIIa și mutațiile genei metilentetrahidrofolat reductază - gena care codifică interleukina-1. În cazul dezvoltării restenozei stentului marginal, principalul factor de risc este o leziune aterosclerotică pronunțată în segmentul stentat.
Restenoza apare predominant în primele 6-8 luni după intervenția coronariană percutanată. Majoritatea pacienților dezvoltă simptome clinice aproximativ în același timp. Restenoza coronariană percutanată (RVS) se manifestă de obicei prin angină recurentă. Angina instabilă apare mai rar (11-41% din cazuri). Infarctul miocardic (IMA) se dezvoltă la 1-6% dintre pacienți. Astfel, cea mai frecventă cauză a anginei pectorale în perioada de 1-6 luni după stentare este dezvoltarea VRS, care, de regulă, necesită revascularizare repetată. Există mai multe metode de tratare a VRS. Se poate efectua angioplastie totală transuretrală (TBCA) convențională, ceea ce duce la o expansiune suplimentară a stentului (contribuție de 56% la creșterea finală a diametrului vasului) și împinge neointima prin celulele stentului (contribuție de 44% la creșterea finală a diametrului). Cu toate acestea, restenoza reziduală se observă în majoritatea cazurilor la locul intervenției (în medie 18%). În plus, după angiografia blocantă a vaselor de sânge (TBCA), revascularizarea repetată este necesară în 11% din cazuri, mai des la pacienții cu boală multivasculară, FEVS scăzută, în cazul intervențiilor pe grefe de bypass venos sau apariției precoce a primei revascularizări venoase (VRS). Riscul de a dezvolta VRS repetate după TBCA depinde, de asemenea, de tipul de leziune și variază de la 10% în cazul restenozei locale până la 80% în cazul ocluziei intra-stent. Implantarea stâlpului inferior de picior (LES) la locul VRS nu reduce riscul de recurență al acestuia în comparație cu TBCA singură.
A doua metodă de tratare a VRS este brahiterapia, care implică introducerea unei surse radioactive în lumenul arterei coronare, prevenind proliferarea celulelor musculare netede și, în consecință, reducând riscul de restenoză. Cu toate acestea, costul ridicat al echipamentului, complexitatea tehnică a procedurii și incidența crescută a trombozei tardive a stentului (LT) au exclus aproape complet brahiterapia din utilizarea clinică.
Un moment revoluționar în tratamentul VRS a fost introducerea stentului medicamentos. Comparativ cu LES în arterele native, acesta reduce riscul de VRS cu 70-80%. Primele date privind eficacitatea DES la pacienții cu VRS deja dezvoltat au fost obținute în registrul de pacienți TAXUS III, în care, atunci când s-a utilizat SPG1 la acești pacienți, frecvența recurenței VRS a fost de doar 16% după 6 luni, ceea ce este mai mic decât în studiile menționate anterior cu TBCA. În registrul TRUE, care a inclus pacienți după implantarea SES pentru restenoza LES, după 9 luni, revascularizarea repetată a fost necesară la mai puțin de 5% dintre pacienți, în principal cu diabet zaharat și SCA. Studiul TROPICAL a comparat frecvența restenozei repetate la pacienți după implantarea DES la locul restenozei cu datele studiilor GAMMA I și GAMMA II, în care brahiterapia a fost utilizată ca metodă de tratament. După 6 luni, incidența restenozei recurente a fost semnificativ mai mică în grupul SPS (9,7 vs 40,3%; p < 0,0001). Este important de menționat că incidența trombozei de stent și a infarctului miocardic a fost, de asemenea, mai mică în grupul SPS (TS 0,6 vs 3,9%; p = 0,08; MI - 1,8 vs 9,4%; p = 0,004). Avantajul SPS față de brahiterapie a fost confirmat în studiul randomizat SISR, în care 384 de pacienți cu VRS dezvoltat în NSC au fost randomizați în grupurile de brahiterapie sau implantare de SPS. După 9 luni, nevoia de revascularizare repetată a fost mai mare după brahiterapie (19,2%) decât în grupul de implantare de SPS (8,5%), ceea ce a reflectat o recurență mai frecventă a restenozei. După 3 ani, avantajul SPS în ceea ce privește reducerea nevoii de revascularizare repetată din cauza restenozei recurente de stent s-a menținut (19 vs 28,4%). Nu a existat nicio diferență semnificativă în ceea ce privește incidența trombozei între grupuri.
Principalii factori pentru dezvoltarea VRS recurentă la pacienții cu LES în cazul implantării de SPS sunt un diametru mic al vasului (< 2,5 mm), tipul difuz de restenoză și prezența insuficienței renale cronice care necesită hemodializă. În studiul randomizat TAXUS V ISR, SPS a demonstrat, de asemenea, o eficiență ridicată în tratamentul VRS, reducând rata restenozei recurente cu 54% în comparație cu brahiterapia.
De asemenea, au fost efectuate studii randomizate care au comparat eficacitatea restenozei repetate a TBCA pentru VRS și implantarea DES. În studiul randomizat RIBS-II, după 9 luni, restenoza repetată a fost cu 72% mai puțin frecventă după implantarea DES decât după TBCA, ceea ce a redus necesitatea revascularizării repetate de la 30 la 11%. Studiul ISAR DESIRE a comparat eficacitatea TBCA pentru VRS cu implantarea SPP sau SPS. După 6 luni, s-a dovedit că ambele DES au fost mai eficiente în prevenirea restenozei repetate decât TBCA (incidența sa a fost de 44,6% cu TBCA, 14,3% în grupul SPS și 21,7% în grupul SPS), ceea ce a redus necesitatea revascularizării repetate. Într-o comparație directă între SPP și SPS, s-a constatat că SPS a redus necesitatea revascularizării repetate semnificativ mai eficient decât SPP (8 vs. 19%). Astfel, implantarea DES reduce incidența VRS recurentă a LES în comparație atât cu TBCA, cât și cu brahiterapia, ceea ce reduce numărul de PCI repetate și, prin urmare, face ca implantarea lor să fie procedura de elecție la acești pacienți.
Restenoză după implantarea unui stent cu eliberare de medicamente (DES)
În ciuda scăderii cu 70-80% a incidenței stenozei intrastent la utilizarea DES în comparație cu LES, nu s-a putut exclude complet dezvoltarea acestei consecințe iatrogene a stentării. Incidența sa generală rămâne, în medie, sub 10%. Pe lângă scăderea cantitativă a incidenței restenozei, s-a modificat semnificativ și tipul de restenoză care apare. Astfel, după implantarea DES, restenoza este de obicei focală. Clinic, ca și în cazul LES, se manifestă cel mai adesea ca o recidivă a anginei stabile (77%), mai rar (8%) este asimptomatică. În 5% din cazuri, se manifestă ca angină instabilă, iar în 10%, primul său simptom este infarctul miocardic fără undă Q. Principalii factori în dezvoltarea restenozei DES sunt diabetul zaharat de tip 2, diametrul mic al vasului și extinderea leziunii. Nu există recomandări clare pentru gestionarea acestor pacienți. Opțiunile alternative sunt reimplantarea unui DES (de același tip sau de unul diferit), angiografia blocantă a arterelor terminale (TBCA) sau brahiterapia. Rata medie de re-restenoză cu un al doilea DES este de 24% și este aceeași dacă se implantează același tip de DES sau unul diferit.


 [
[