
Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Patogeneza hepatitei B
Expert medical al articolului
Ultima examinare: 07.07.2025
În patogeneza hepatitei B, pot fi identificate mai multe verigi principale în lanțul patogenetic:
- introducerea agentului patogen - infecția;
- fixarea pe hepatocit și pătrunderea în celulă;
- multiplicarea virusului și „împingerea” acestuia pe suprafața hepatocitelor, precum și în sânge;
- activarea reacțiilor imunologice care vizează eliminarea agentului patogen;
- afectarea complexelor imune a organelor și sistemelor;
- formarea imunității, eliberarea de agentul patogen, vindecare.
Întrucât infecția cu hepatita B are loc întotdeauna parenteral, se poate considera că momentul infecției este practic echivalent cu pătrunderea virusului în sânge. Încercările unor cercetători de a distinge fazele enterale și regionale în hepatita B sunt slab fundamentate. Există mai multe motive pentru a crede că virusul pătrunde imediat în ficat odată cu fluxul sanguin.
Tropismul virusului hepatitei B la nivelul țesutului hepatic este predeterminat de prezența unui receptor special în HBsAg - un polipeptid cu o greutate moleculară de 31.000 Da (P31), care are activitate de legare a albuminei. O zonă similară de albumină se găsește și pe membrana hepatocitelor din ficatul oamenilor și cimpanzeilor, care determină în esență tropismul HBV la nivelul ficatului oamenilor și cimpanzeilor.
Când virusul pătrunde în hepatocit, se eliberează ADN viral, care, intrând în nucleul hepatocitului și acționând ca o matrice pentru sinteza acizilor nucleici, declanșează o serie de reacții biologice secvențiale, al căror rezultat este asamblarea nucleocapsidei virusului. Nucleocapsida migrează prin membrana nucleară în citoplasmă, unde are loc asamblarea finală a particulelor Dane - virusul hepatitei B complet.
Trebuie menționat, totuși, că atunci când un hepatocit este infectat, procesul poate decurge în două moduri - replicativ și integrativ. În primul caz, se dezvoltă o imagine de hepatită acută sau cronică, iar în al doilea - purtător de virus.
Motivele care determină cele două tipuri de interacțiune dintre ADN-ul viral și hepatocite nu au fost stabilite cu precizie. Cel mai probabil, tipul de răspuns este determinat genetic.
Rezultatul interacțiunii replicative este asamblarea structurilor antigenice centrale (în nucleu) și asamblarea virusului complet (în citoplasmă), urmată de prezentarea virusului complet sau a antigenelor sale pe membrană sau în structura membranei hepatocitelor.
În general, este acceptat faptul că replicarea virusului nu are ca rezultat deteriorarea celulară la nivel hepatocitar, deoarece virusul hepatitei B nu are efect citopatic. Această poziție nu poate fi considerată incontestabilă, deoarece se bazează pe date experimentale care, deși indică absența unui efect citopatic al virusului hepatitei B, au fost obținute pe culturi de țesuturi și, prin urmare, nu pot fi extrapolate complet la hepatita virală B la om. În orice caz, problema absenței afectării hepatocitelor în timpul fazei replicative necesită studii suplimentare.
Totuși, indiferent de natura interacțiunii virusului cu celula, ficatul este în mod necesar inclus în procesul imunopatologic. În acest caz, afectarea hepatocitelor este asociată cu faptul că, în urma exprimării antigenelor virale pe membrana hepatocitelor și a eliberării antigenelor virale în circulație liberă, este inclus un lanț de reacții imune celulare și umorale secvențiale, care vizează în final eliminarea virusului din organism. Acest proces se desfășoară în deplină conformitate cu tiparele generale ale răspunsului imun la infecțiile virale. Pentru eliminarea agentului patogen, sunt incluse reacții citotoxice celulare, mediate de diverse clase de celule efectoare: celule K, celule T, ucigași naturali, macrofage. În timpul acestor reacții, hepatocitele infectate sunt distruse, ceea ce este însoțit de eliberarea de antigene virale (HBcAg, HBeAg, HBsAg), care declanșează sistemul de geneză a anticorpilor, în urma căruia se acumulează anticorpi specifici în sânge, în principal la nivelul nucleului - anti-HBc și e-antigenului - anti-HBE. În consecință, eliberarea celulei hepatice din virus are loc în procesul morții sale datorită reacțiilor de citoliză celulară.
În același timp, anticorpii specifici care se acumulează în sânge se leagă de antigenele virale, formând complexe imune fagocitate de macrofage și excretate prin rinichi. În acest caz, pot apărea diverse leziuni ale complexelor imune sub formă de glomerulonefrită, arterită, artralgie, erupții cutanate etc. Cu participarea anticorpilor specifici, organismul este curățat de agentul patogen și are loc recuperarea completă.
În conformitate cu conceptul conturat al patogenezei hepatitei B, întreaga diversitate a variantelor clinice ale evoluției bolii este de obicei explicată prin particularitățile interacțiunii virusului și cooperarea celulelor imunocompetente, cu alte cuvinte, prin puterea răspunsului imun la prezența antigenelor virale. Conform conceptelor moderne, puterea răspunsului imun este determinată genetic și legată de antigenele de histocompatibilitate ale locusului HLA de prima clasă.
În general, se acceptă faptul că, în condițiile unui răspuns imun adecvat la antigenele virale, hepatita acută se dezvoltă clinic, cu un curs ciclic și recuperare completă. Pe fondul scăderii răspunsului imun la antigenele virale, citoliza mediată imun este exprimată nesemnificativ, prin urmare, nu există o eliminare eficientă a celulelor hepatice infectate, ceea ce duce la manifestări clinice ușoare, cu persistența pe termen lung a virusului și, eventual, la dezvoltarea hepatitei cronice. În același timp, dimpotrivă, în cazul unui răspuns imun puternic determinat genetic și a unei infecții masive (hemotransfuzie), apar zone extinse de afectare a celulelor hepatice, care corespund clinic formelor severe și maligne ale bolii.
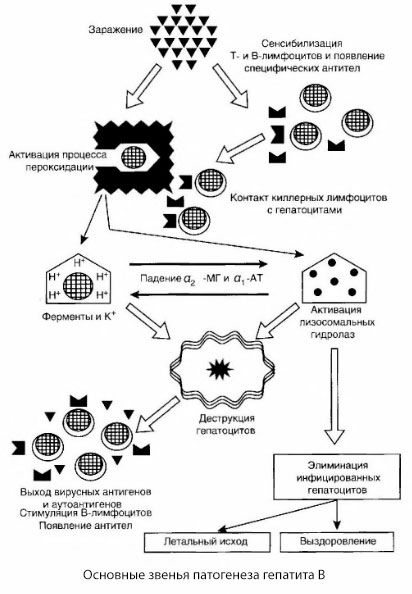
Schema prezentată a patogenezei hepatitei B se distinge prin coerența sa; cu toate acestea, conține o serie de puncte controversate și slab studiate.
Dacă urmăm conceptul de hepatită B ca boală imunopatologică, ne putem aștepta la o creștere a reacțiilor de citotoxicitate celulară odată cu creșterea severității bolii. Cu toate acestea, în formele severe, indicii legăturii celulare a imunității sunt reduși drastic, inclusiv o scădere multiplă, comparativ cu cei la copiii sănătoși, și indicele de citotoxicitate al celulelor K. În forma malignă, în perioada de dezvoltare a necrozei hepatice masive și în special a comei hepatice, se observă o incapacitate completă a limfocitelor de a se transforma în blastici sub influența fitohemaglutininei, endotoxinei stafilococice și HBsAg. În plus, nu există capacitatea leucocitelor de a migra conform reacției de inhibare a migrării leucocitelor (LMIC), iar rezultatele studiilor efectuate cu o sondă fluorescentă de tetraciclină relevă o creștere bruscă a permeabilității membranelor limfocitare.
Astfel, dacă indicii de fluorescență ai limfocitelor la persoanele sănătoase sunt de 9,9±2%, iar în hepatita B tipică cu evoluție benignă cresc la 22,3±2,7%, atunci în formele maligne numărul de limfocite fluorescente atinge o medie de 63,5±5,8%. Întrucât creșterea permeabilității membranelor celulare este evaluată fără echivoc în literatura de specialitate ca un indicator fiabil al inferiorității lor funcționale, se poate concluziona că în cazul hepatitei B, în special în forma malignă, există o afectare macroscopică a limfocitelor. Acest lucru este evidențiat și de indicii citotoxicității celulelor K. În forma severă, în săptămâna 1-2 a bolii, citotoxicitatea este de 15,5±8,8%, iar în forma malignă în prima săptămână - 6,0±2,6, în a 2-a - 22,0±6,3% cu o normă de 44,8±2,6%.
Datele prezentate indică în mod clar perturbări pronunțate ale legăturii celulare a imunității la pacienții cu forme severe de hepatită B. De asemenea, este evident că aceste modificări apar secundar, ca urmare a deteriorării celulelor imunocompetente de către metaboliți toxici și, eventual, complexe imune circulante.
După cum au arătat studiile, la pacienții cu forme severe de hepatită B, în special în cazul dezvoltării necrozei hepatice masive, titrul de HBsAg și HBeAg din serul sanguin scade și, în același timp, anticorpii împotriva antigenului de suprafață încep să fie detectați în titruri ridicate, ceea ce este complet necaracteristic pentru formele benigne ale bolii, în care anticorpii anti-HBV apar abia în lunile 3-5 ale bolii.
Dispariția rapidă a antigenelor virusului hepatitei B, cu apariția simultană a unor titruri ridicate de anticorpi antivirali, sugerează formarea intensivă a complexelor imune și posibila lor participare la patogeneza dezvoltării necrozei hepatice masive.
Prin urmare, materialele factuale nu ne permit să interpretăm hepatita B în mod lipsit de echivoc doar din punctul de vedere al agresiunii imunopatologice. Și ideea nu este doar că nu se găsește nicio legătură între profunzimea și prevalența modificărilor morfologice din ficat, pe de o parte, și severitatea factorilor imunității celulare, pe de altă parte. Teoretic, această circumstanță ar putea fi explicată prin etapele târzii ale studiului indicatorilor imunității celulare, când celulele imunocompetente au fost supuse unor efecte toxice puternice din cauza creșterii insuficienței funcționale a ficatului. Desigur, se poate presupune că citoliza imună a hepatocitelor are loc în cele mai timpurii etape ale procesului infecțios, posibil chiar înainte de apariția simptomelor clinice de afectare hepatică severă. Cu toate acestea, o astfel de presupunere este puțin probabilă, deoarece indicatori similari ai imunității celulare au fost detectați la pacienții cu cea mai acută (fulger) evoluție a bolii și, în plus, în timpul examinării morfologice a țesutului hepatic, nu s-a detectat infiltrare limfocitară masivă, în timp ce, în același timp, s-au detectat câmpuri continue de epiteliu necrotic fără fenomenele de resorbție și agresiune limfocitară.
Este foarte dificil să explicăm tabloul morfologic al hepatitei acute doar din punctul de vedere al citolizei celulare imune, prin urmare, în studiile timpurii, efectul citotoxic al virusului hepatitei B nu a fost exclus.
În prezent, această presupunere a fost parțial confirmată de descoperirea virusului hepatitei B. După cum au arătat studiile, frecvența detectării markerilor hepatitei D depinde direct de severitatea bolii: în formele ușoare, aceștia sunt detectați la 14%, moderate - la 18%, severe - 30% și maligne - la 52% dintre pacienți. Având în vedere că virusul hepatitei D are un efect citopatic necrozogen, se poate considera stabilit că coinfecția cu virusurile hepatitei B și D este de mare importanță în dezvoltarea formelor fulminante de hepatită B.
Patogeneza hepatitei B poate fi prezentată după cum urmează. După pătrunderea virusului hepatitei B în hepatocite, un atac imunologic asupra hepatocitelor infectate este indus de T-killer-i, care secretă limfotoxine în direcția celulelor hepatice.
Mecanismele intime ale afectării hepatocitelor în hepatita B nu au fost încă stabilite. Rolul principal este jucat de procesele activate de peroxidare lipidică și hidrolaze lizozomale. Factorul declanșator poate fi limfotoxinele eliberate de celulele efectoare la contactul lor cu hepatocitele, dar este posibil ca virusul însuși să fie inițiatorul proceselor de peroxidare. Ulterior, procesul patologic se dezvoltă cel mai probabil în următoarea secvență.
- Interacțiunea factorului de agresivitate (limfotoxine sau virusuri) cu macromolecule biologice (posibil cu componente ale membranelor reticulului endoplasmatic capabile să participe la procesele de detoxifiere, prin analogie cu alți agenți nocivi, așa cum s-a demonstrat în cazul tetraclorurii de carbon).
- Formarea radicalilor liberi, activarea proceselor de peroxidare lipidică și creșterea permeabilității tuturor membranelor hepatocelulare (sindromul de citoliză).
- Mișcarea substanțelor biologic active de-a lungul gradientului de concentrație - pierderea enzimelor cu diferite localizări intracelulare, donori de energie, potasiu etc. Acumularea de sodiu și calciu în celule, schimbarea pH-ului către acidoză intracelulară.
- Activarea și eliberarea hidrolazelor lizozomale (ARNază, ADNază, catepsine etc.) cu descompunerea celulelor hepatice și eliberarea autoantigenelor.
- Stimularea sistemelor imune T și B cu formarea unei sensibilizări specifice a limfocitelor T la lipoproteinele hepatice, precum și formarea de autoanticorpi umorali antihepatici.
În schema propusă a patogenezei hepatitei B, factorul declanșator îl reprezintă antigenele virale, a căror producție intensivă se observă în stadiile incipiente ale bolii și pe tot parcursul perioadei acute, cu excepția formelor maligne, în care producția de antigene virale practic încetează în momentul dezvoltării necrozei hepatice masive, ceea ce predetermină o scădere rapidă a replicării virale.
De asemenea, este evident că antigenele virale activează sistemele imune T și B. În timpul acestui proces, are loc o redistribuire caracteristică a subpopulațiilor de limfocite T, care vizează organizarea unui răspuns imun adecvat, eliminarea hepatocitelor infectate, neutralizarea antigenelor virale, sanogeneza și recuperarea.
Când celulele imunocompetente interacționează cu antigenele virale de pe membranele hepatocitelor sau în timpul reproducerii virusului în interiorul unui hepatocit, apar condiții pentru activarea proceselor de peroxidare lipidică, care, după cum se știe, controlează permeabilitatea tuturor membranelor celulare și subcelulare.
Din această poziție, apariția sindromului de citoliză, o permeabilitate crescută a membranelor celulare, atât de naturală și caracteristică hepatitei virale, devine de înțeles.
Rezultatul final al sindromului de citoliză poate fi decuplarea completă a fosforilării oxidative, scurgerea de material celular și moartea parenchimului hepatic.
Totuși, în marea majoritate a cazurilor, aceste procese nu dobândesc o dezvoltare atât de fatală. Numai în formele maligne ale bolii procesul patologic se desfășoară într-o manieră asemănătoare avalanșei și ireversibil, deoarece apar infecții masive, un proces imun pronunțat, activarea excesivă a proceselor de peroxidare și a hidrodazelor lizozomale și fenomene de agresiune autoimună.
Aceleași mecanisme se observă și în evoluția favorabilă a hepatitei B, cu singura particularitate că toate se realizează la un nivel calitativ diferit. Spre deosebire de cazurile de necroză hepatică masivă, în evoluția favorabilă a bolii numărul de hepatocite infectate și, prin urmare, zona de citoliză imunopatologică este mai mic, procesele de peroxidare lipidică nu sunt la fel de semnificativ amplificate, activarea hidrolazelor acide duce doar la o autoliză limitată cu o eliberare nesemnificativă de autoantigene și, prin urmare, fără autoagresiune masivă, adică toate etapele patogenezei în evoluția favorabilă se desfășoară în cadrul organizării structurale conservate a parenchimului hepatic și sunt restricționate de sistemele de apărare (antioxidanți, inhibitori etc.) și, prin urmare, nu au un efect atât de distructiv.
Cauzele simptomelor de intoxicație în hepatita virală nu au fost studiate pe deplin. Propunerea de a distinge între așa-numita intoxicație primară sau virală și cea secundară (de schimb sau metabolică) poate fi considerată pozitivă, deși aceasta nu dezvăluie mecanismul intim al apariției sindromului toxic general. În primul rând, virusurile hepatitice nu au proprietăți toxice, iar în al doilea rând, concentrația multor metaboliți nu se corelează întotdeauna cu severitatea bolii și gradul de exprimare a simptomelor de toxicoză. De asemenea, se știe că concentrația antigenelor virale nu se corelează strict cu severitatea intoxicației. Dimpotrivă, odată cu creșterea severității bolii și, prin urmare, cu creșterea gradului de toxicoză, concentrația de HBsAg scade și este cea mai mică în formele maligne în momentul debutului comei hepatice profunde. În același timp, frecvența detectării și titrurile anticorpilor antivirali specifici depind direct de severitatea bolii.

Intoxicația nu apare în momentul înregistrării antigenelor virale, ci în perioada de circulație în sânge a anticorpilor antivirali de clasa IgM împotriva antigenului de vacă și a antigenului sistemului E. Mai mult, în formele severe și în special maligne, o proporție semnificativă de pacienți au chiar anticorpi anti-HBs în sânge, ceea ce de obicei nu se observă niciodată în formele ușoare și moderate ale bolii.
Datele prezentate ne permit să concluzionăm că sindromul toxicotic în hepatita virală, și în special în hepatita B, nu apare ca urmare a apariției antigenelor virale în sânge, ci este o consecință a interacțiunii antigenelor virale cu anticorpii antivirali din clasa IgM. Rezultatul unei astfel de interacțiuni, după cum se știe, este formarea de complexe imune și, eventual, substanțe toxice active.
Simptomele intoxicației apar în momentul apariției complexelor imune în circulație liberă, dar ulterior o astfel de corelație nu se observă.
O explicație parțială pentru aceasta poate fi găsită în studiul compoziției complexelor imune. La pacienții cu forme severe, în sânge circulă predominant complexe de dimensiuni medii, iar în compoziția lor, în punctul culminant al sindromului toxic, predomină anticorpii din această clasă, în timp ce în perioada de declin al manifestărilor clinice și de convalescență, complexele devin mai mari, iar în compoziția lor încep să predomine anticorpii din clasa IgG.
Datele prezentate se referă la mecanismele de dezvoltare a sindromului toxic în perioada inițială a bolii, însă în toxicozele apărute în punctul culminant al manifestărilor clinice, acestea au doar o semnificație parțială, în special în dezvoltarea comei hepatice.

Metoda hemoculturilor a arătat că, în cazul hepatitei B, toxinele se acumulează constant în sânge, fiind eliberate din țesutul hepatic deteriorat și în descompunere. Concentrația acestor toxine este proporțională cu severitatea bolii, fiind de natură proteică.
În perioada de recuperare, anticorpii la această toxină apar în sânge; dar în cazul comei hepatice, concentrația toxinei din sânge crește brusc, iar anticorpii nu sunt detectați în sânge.

Patomorfologia hepatitei B
Pe baza naturii modificărilor morfologice, se disting trei forme de hepatită acută B:
- formă ciclică,
- necroză hepatică masivă;
- hepatita pericolangiolitică colestatică.
În forma ciclică a hepatitei B, modificările distrofice, inflamatorii și proliferative sunt mai pronunțate în centrul lobulilor, în timp ce în hepatita A acestea sunt localizate de-a lungul periferiei lobulilor, răspândindu-se spre centru. Aceste diferențe se explică prin diferitele căi de penetrare a virusului în parenchimul hepatic. Virusul hepatitei A pătrunde în ficat prin vena portă și se răspândește spre centrul lobulilor, virusul hepatitei B pătrunde prin artera hepatică și ramurile capilare care vascularizează uniform toți lobulii, chiar până la centrul lor.
Gradul de afectare a parenchimului hepatic corespunde în majoritatea cazurilor severității manifestărilor clinice ale bolii. În formele ușoare, se observă de obicei necroza focală a hepatocitelor, iar în formele moderate și severe - necroza zonală (cu tendința de a se contopi și forma necroză de tip punte în formele severe ale bolii).
Cele mai mari modificări morfologice ale parenchimului se observă în punctul culminant al manifestărilor clinice, care coincide de obicei cu prima decadă a bolii. În timpul celei de-a doua și mai ales a celei de-a treia decade, procesele de regenerare se intensifică. În această perioadă, modificările necrobiotice dispar aproape complet și încep să predomine procesele de infiltrare celulară, cu o restaurare ulterioară lentă a structurii plăcilor hepatocelulare. Cu toate acestea, restaurarea completă a structurii și funcției parenchimului hepatic are loc abia la 3-6 luni de la debutul bolii și nu la toți pacienții.
Natura generalizată a infecției în hepatita B este confirmată de detectarea HBsAg nu numai în hepatocite, ci și în rinichi, plămâni, splină, pancreas, celule ale măduvei osoase etc.
Hepatita colestatică (pericolangiolitică) este o formă specială a bolii, în care cele mai mari modificări morfologice se observă la nivelul canalelor biliare intrahepatice, cu o imagine de colangiolită și pericololangiolită. În forma colestatică, colestaza apare cu dilatarea capilarelor biliare cu stază a bilei în ele, cu proliferarea colangiolei și infiltrate celulare în jurul lor. Celulele hepatice sunt afectate nesemnificativ în această formă de hepatită. Clinic, boala se caracterizează printr-o evoluție prelungită cu icter prelungit. S-a demonstrat că cauza unei astfel de evoluții particulare a bolii este efectul predominant al virusului asupra pereților colangiolei, cu un efect nesemnificativ asupra hepatocitelor.

